13.某同学设计如下四个实验来验证Fe.Cu.Ag三种金属的活动性.其中不必进行的是 A.将铁片放入稀盐酸 B.将铜片放入稀盐酸C.将银片放入稀盐酸 D.将铜片放入硝酸银溶液 【
查看更多】
题目列表(包括答案和解析)
某同学设计如下四个实验来验证Fe、Cu、Ag三种金属的活动性.其中不必进行的是( )
查看答案和解析>>
某同学设计如下四个实验来验证Fe、Cu、Ag三种金属的活动性。其中不必进行的是
A.将铁片放入稀盐酸
B.将铜片放入稀盐酸
C.将银片放入稀盐酸
D.将铜片放入硝酸银溶液
查看答案和解析>>
归纳与整理是化学学习的一种重要方法.
(1)某化学活动小组以“酸碱盐的性质”为主题进行探究性学习,请你来解决下列问题:
A.小红同学从某一欠收农田里取回一份土壤样品,如果检测结果呈酸性,从经济和可行方面考虑,那么要改良此土壤的酸性,应向农田里施加
Ca(OH)2
Ca(OH)2
(填化学式).
B.小红同学用图1总结了NaOH的四条化学性质(即NaOH与四类物质能够发生化学反应).
I.为了验证反应①,小红将无色酚酞试液滴入NaOH溶液中,溶液由无色变成
红色
红色
.
II.依据反应④说明NaOH必须密封保存,否则在空气中要变质,其化学反应方程式为:
CO2+2NaOH=Na2CO3+H2O
CO2+2NaOH=Na2CO3+H2O
.
III.为了验证反应③能够发生,你选择的物质是
c
c
.
a.Na
2CO
3 b.HCl c.FeCl
3 d.Ba(NO
3)
2C.请你设计一个实验除去FeCl
2溶液中少量的CuCl
2,请写出主要操作步骤和化学方程式.实验主要操作步骤:
取溶液于试管中加入过量铁粉
取溶液于试管中加入过量铁粉
、
过滤
过滤
,化学方程式:
CuCl2+Fe=FeCl2+Cu
CuCl2+Fe=FeCl2+Cu
.
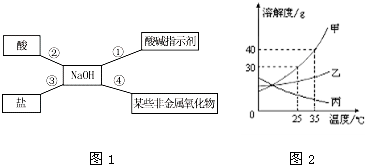
(2)甲、乙、丙三种固体物质的溶解度曲线如图2所示,请回答:
①25℃时,将25g甲固体加入到50g水中,充分溶解并恢复到原温度后,得到溶液的质量为
65
65
g.
②要使35℃时接近饱和的甲溶液变成该温度下的饱和溶液,可采用的一种方法是
加入甲物质(溶质)至不再溶解
加入甲物质(溶质)至不再溶解
.
③现有操作步骤:a.溶解 b.过滤 c.降温结晶 d.加热浓缩;若甲固体中含有少量乙,则提纯甲的操作步骤是
adcb
adcb
(填字母序号).
④将35℃时丙的饱和溶液降温到25℃,则其溶液的溶质质量分数
不变
不变
(填“变大”、“变小”或“不变”).
⑤向100g35℃的水中加入45g甲固体,发现全部溶解,一段时间后又有部分甲的晶体析出.你认为“全部溶解”的原因可能是
甲固体溶于水时放热
甲固体溶于水时放热
.
查看答案和解析>>
某化学活动小组以“酸碱盐的性质”为主题进行探究性学习,请你作为该小组成员一起来解决下列问题:
(1)小红同学从某一欠收农田里取回一份土壤样品,如果检测结果呈酸性,从经济和可行方面考虑,那么要改良此土壤的酸性,应向农田里施加 (填化学式)
Ca(OH)2
Ca(OH)2
.
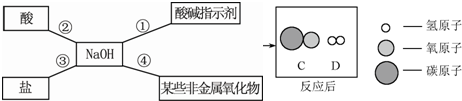
(2)小红同学用下图总结了NaOH的四条化学性质(即NaOH与四类物质能够发生化学反应).
I依据反应④说明NaOH必须密封保存,否则在空气中要变质,其化学反应方程式为:
CO2+2NaOH=Na2CO3+H2O
CO2+2NaOH=Na2CO3+H2O
.
II为了验证反应③能够发生,你选择的物质是
c
c
(填序号).
a.Na
2CO
3 b.HCl c.CuSO
4 d.CO
2(3)请你设计一个实验除去FeCl
2溶液中少量的CuCl
2,写出化学方程式:
CuCl2+Fe═FeCl2+Cu
CuCl2+Fe═FeCl2+Cu
.
查看答案和解析>>
某化学活动小组以“酸碱盐的性质”为主题进行探究性学习,请你作为该小组成员一起来解决下列问题:
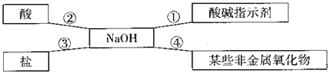
(1)小红同学用如图总结了NaOH的四条化学性质.(即NaOH与四类物质能够发生化学反应)
Ⅰ、为了验证反应①,小红将无色酚酞试液滴入NaOH溶液中,溶液由无色变成
红色
红色
.
Ⅱ、依据反应④说明NaOH必须密封保存,否则在空气中要变质,其化学反应方程式为
CO2+2NaOH=Na2CO3+H2O
CO2+2NaOH=Na2CO3+H2O
.
Ⅲ、为了验证反应③能够发生,你选择的物质是
C
C
.
a、Na
2CO
3 b、HCl c、FeCl
3 d、Ba(NO)
2
(2)请你设计一个实验除去FeCl
2溶液中少量的CuCl
2,写出主要操作步骤和化学方程式:
实验主要操作步骤:
取溶液于试管中加入过量铁粉;
取溶液于试管中加入过量铁粉;
、
过滤
过滤
;
化学方程式:
CuCl2+Fe=FeCl2+Cu
CuCl2+Fe=FeCl2+Cu
.
查看答案和解析>>
2009.5
一、选择题(每小题1分,共25分)
题号
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
答案
D
B
A
B
A
D
B
B
D
A
C
C
C
D
D
题号
16
17
18
19
20
21
22
23
24
25
|
答案 D C D C A C C D A D |
说明:以下各题若有其他正确答案,均可得分。
二、填空题(除29题(1)小题2分外,每空1分,共29分)
26.(6分)
(1)①糖类、油脂、蛋白质;②锌。 (2)①钙,②A。 (3)①0.4,②1.1。
27.(7分)
(1)A。 (2)①蒸馏。②乳化。(3)①甲。②b,
③升温(或增加溶剂)。④不变。
 28.(7分)
28.(7分)
 (1)A。
(2)①混合物。 ②生铁的含碳量比钢高。 ③3CO + Fe2O3 3CO2 + 2Fe 。
(1)A。
(2)①混合物。 ②生铁的含碳量比钢高。 ③3CO + Fe2O3 3CO2 + 2Fe 。
(3)FeCl2 + H2 Fe + 2HCl (4)①Fe + CuCl2 = FeCl2
+ Cu ;②Fe 、Cu。
29.(4分)
(1)B、C、D、E。(全部选对得2分,少选1个且无错误选项得1分)
(2)Na+、Cl-、H2O。
(3)⑤④①②③。
 30.(5分)
30.(5分)
(1)①O2; ②2H2O 2H2↑+ O2↑; ③Ca(OH)2+ CO2= CaCO3↓+ H2O
(2)①置换反应, ②Fe + H2SO4= FeSO4 + H2↑。
三、实验题(每空1分,共19分)
 31.(6分)
31.(6分)
(1)①2KMnO4 K2MnO4
+ MnO2 + O2↑,②A。 ③将带火星的木条置于集气瓶口,若木条复燃,则氧气已满。
(2)①B、C, ②能, ③氧气和二氧化碳均可以由固体和液体药品在常温条件下反应制得,且它们的密度均大于空气。
32.(7分)
(1)①稀盐酸
②Na2CO3 ③滴加步骤2检验出的溶液。 ④一支试管溶液中有白色沉淀生成,则原溶液是Ca(OH)2溶液;另一支试管无明显现象,则原溶液是NaOH溶液。⑤ Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
(2)①小伟, ②Ca(OH)2。
33.(6分)
①氧气 ②部分溶解,产生无色气泡,(溶液为浅绿色)。 ③氧化铁。
④Fe2O3+ 6HCl = 2FeCl3 + 3H2O
⑤取适量A袋内物质于烧杯内,加入过量稀盐酸,充分反应后过滤,洗涤、烘干滤渣。点燃滤渣,将产生的气体通入澄清石灰水,若产生能使澄清石灰水变浑浊的气体,则剩余物质中还含有活性炭。[答案合理即给分]
⑥保存“暖宝宝”取暖贴时不要使外袋破损,保持包装的气密性,以防失效。
四、计算题(共7分)
34.(3分)
 [解]设:需要O2的质量为x。
[解]设:需要O2的质量为x。
2H2+ O2
2H2O
……………………………………(1分)
 4 32
4 32
4
8 g = 
x = 64 g
……………………………………(1分) 答:需要O2的质量为64 g。 35.(4分) (1)3 (2)根据表中数据可知样品中铁的质量为6.0 g-0. 4 g=5. 6 g 单质铁的质量分数= ×100% = 93.3% ×100% = 93.3% (3)[解]设:生成H2的质量为x。 Fe+H2SO4=FeSO4+H2↑ 56
152 2
2
5.6 g 56 y = 15.2 g x= 0.2 g = x =   x = 0. x = 0.

反应后溶液中溶质的质量分数为
×100%=33.5%
(4)C
| | | | | | | |



 某化学活动小组以“酸碱盐的性质”为主题进行探究性学习,请你作为该小组成员一起来解决下列问题:
某化学活动小组以“酸碱盐的性质”为主题进行探究性学习,请你作为该小组成员一起来解决下列问题: 28.(7分)
28.(7分) (1)A。
(2)①混合物。 ②生铁的含碳量比钢高。 ③3CO + Fe2O3 3CO2 + 2Fe 。
(1)A。
(2)①混合物。 ②生铁的含碳量比钢高。 ③3CO + Fe2O3 3CO2 + 2Fe 。 30.(5分)
30.(5分) 31.(6分)
31.(6分) [解]设:需要O2的质量为x。
[解]设:需要O2的质量为x。 4 32
4 32