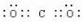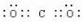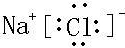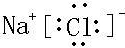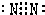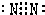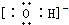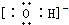填写空格
(1)写出下列物质的电子式:N
2;HClO
;
(2)写出下列物质的结构式:CH
4; CO
2O═C═O
O═C═O
.
(3)与Ar原子电子层结构相同的-2价阴离子的离子结构示意图
.
(4)在1-18号元素组成的化合物中具有三核10个电子的共价化合物是
H2O
H2O
;具有三核20个电子的离子化合物是
LiHS或NaOH
LiHS或NaOH
;具有四核18个电子的两种化合物分别是
H2O2
H2O2
、
PH3
PH3
;既具有离子键又有非极性键和极性键的化合物是
CH3COONa
CH3COONa
.
(5)下列叙述中所涉及元素是氧元素的有
abcdeg
abcdeg
a.质量数为18,原子核中有10个中子的核素
b.核电荷数等于最外层电子数的离子
c.质子数等于短周期同族元素原子序数一半的元素
d.原子的最外层电子数是内层电子数3倍的元素
e.能与H、C、N、Na、S、Fe等元素形成两种或两种以上的化合物的元素
f.形成化合物的种类最多的元素
g.Y和Z均由元素R组成,反应Y+2I
-+2H
+
I
2+Z+H
2O,其中的R元素.



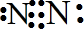
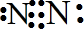


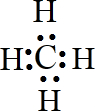
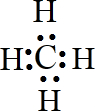




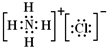
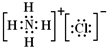






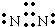
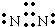






 I2+Z+H2O,其中的R元素.
I2+Z+H2O,其中的R元素.