
题目列表(包括答案和解析)
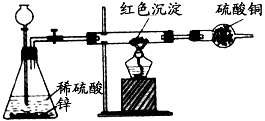
(13分)光气学名“碳酰氯”,化学式COCl2,是窒息性毒剂之一。
2-1 光气化学性质活泼,具有酰卤的典型反应,易发生水解、氨解和醇解。
(1)光气与足量乙醇反应所得产物的化学名称是 ;
(2)光气与足量氨气反应的化学方程式 ;
(3)足量苯在AlCl3催化剂作用下与光气反应所得产物的结构简式 ;
(4)光气与苯胺分两步反应可得异氰酸苯酯,中间产物的结构简式是 ,异氰酸苯酯的结构简式是 。
2-2 实验室可用四氯化碳和发烟硫酸(H2SO4?SO3)反应制备光气,写出化学方程式。
2-3 BTC是一种稳定的白色结晶体,熔点为78~82℃,沸点为203~206℃。1mol BTC可在一定条件下分解产生3mol光气,所以又被称为“三光气”。工业上可以利用碳酸二甲酯的氯代反应制备BTC。BTC的反应活性与光气类似,可以和醇、醛、胺、酰胺、羧酸、酚、羟胺等多种化合物反应,因此低毒性的BTC在化学反应中完全可替代剧毒(被禁用)的光气合成相关的化工产品。
(1)BTC分子中所有氯原子都等价,试写出结构简式
(2)除毒性外,BTC比光气还有什么优点?
2-4 2004年6月15日福建省物质结构研究所(简称物构所)一下属企业,因实验操作不当造成有毒光气泄漏。造成1人死亡,260多人送医院救治。光气遇热按照下式分解:COCl2(g)=CO(g)+Cl2(g),Kp=4.44×10-2(668K,K为标准平衡常数),在密闭容器中,当混合气体总压力为300kPa时,计算该混合气体的平均分子量。
(08上海建平中学期末)国家质检总局查处了在食品中使用“雕白块”七大案例。“雕白块”的化学名称为甲醛次硫酸氢钠(NaHSO2?CH2O),违法者往食品中添加“雕白块”是为了漂白增色、防腐、增加米面制品的韧性及口感。但人食用“雕白块”后会刺激肠道,引起过敏和食物中毒,容易致癌。已知“雕白块”是甲醛和次硫酸氢钠(可表示成Na+[OSOH]-)反应制得:
![]()
回答下列问题:
(1)“雕白块”_______________(填“易”或“微”或“难”)溶于水。“雕白块”具有________(填“强还原性”或“强氧化性”), 已知“雕白块”溶液中滴加足量碘水反应生成的产物中有甲醛,写出化学方程式_____________________________________。
(2)写出次硫酸氢根的电子式___________________________。
(3)写出水溶液中次硫酸氢钠和氢氧化钾反应的离子方程式__ 。
(4)甲醛能使__________变性凝固,所以可用其浓溶液保存动物标本。
(5)甲醛是非常重要的合成原料。纯净的甲醛在[F3B←O(CH2CH3)2]配位化合物的催化下,加聚生成聚甲醛(是一种优良的工程塑料),聚甲醛的结构简式为_____________;俄国化学家布特列洛夫在1861年首次发现在弱碱作用下,6个甲醛分子加合得到己糖,此己糖的分子式为___________。
(6)已知
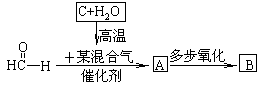
其中A可还原新制的氢氧化铜悬浊液,亦可与乙酸发生酯化反应;B的相对分子质量是甲醛的整数倍,自然界中常以盐的形式存在于多种植物的细胞膜中,B可洗除衣物上的铁锈渍。完成下列填空:
A的同分异构体有(写出结构简式)__________________________________。
A催化加氢的化学方程式____________________________________________。
B可被酸性高锰酸钾溶液氧化,写出B跟稀硫酸、高锰酸钾混合溶液反应的反应式_____
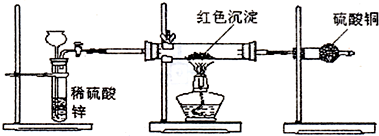
电解是最强有力的氧化还原手段,在化工生产中有着重要的应用。请回答下列问题:
(1)以铜为阳极,以石墨为阴极,用NaCl溶液作电解液进行电解,得到半导体材料Cu2O和一种清洁能源,则阳极反应式为________,阴极反应式为________。
(2)某同学设计如图所示的装置探究金属的腐蚀情况。下列判断合理的是
_______(填序号)。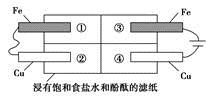
a.②区铜片上有气泡产生
b.③区铁片的电极反应式为2Cl--2e-=Cl2↑
c.最先观察到变成红色的区域是②区
d.②区和④区中铜片的质量均不发生变化
(3)最新研究发现,用隔膜电解法处理高浓度乙醛废水的工艺具有流程简单、能耗较低等优点,其原理是使乙醛分别在阴、阳极发生反应生成乙醇和乙酸,总反应式为2CH3CHO+H2OCH3CH2OH+CH3COOH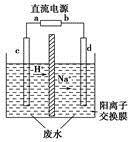
实验室中,以一定浓度的乙醛-Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置如图所示。
①若以甲烷碱性燃料电池为直流电源,则燃料电池中b极应通入________(填化学式),电极反应式为________。电解过程中,阴极区Na2SO4的物质的量________(填“增大”、“减小”或“不变”)。
②在实际工艺处理中,阴极区乙醛的去除率可达60%。若在两极区分别注入1 m3乙醛含量为3 000 mg/L的废水,可得到乙醇________kg(计算结果保留小数点后一位)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com