
题目列表(包括答案和解析)
依照阿伏加德罗定律,下列叙述正确的是
( ) A.同温同压下两种气体的体积之比等于摩尔质量之比。
B.同温同压下两种气体的物质的量之比等于密度之比。 C.同温同压下两种气体的摩尔质量之比等于密度之比。D.同温同体积下两种气体的物质的量之比等于压强之比。
设NA表示阿伏加德罗常数,下列说法不正确的是 ( )
A. 醋酸的摩尔质量与NA个醋酸分子的质量在数值上相等。
B.标准状况下,以任意比混和的氢气和一氧化碳气体共8.96L,在足量氧气中充分燃烧时消耗氧气的分子数为0.2 NA。
C.1L1mol/LCuCl2溶液中含有的Cu2+的个数为NA。
D.25℃,1.01×105Pa时,16g臭氧所含的原子数为NA。
设NA表示阿伏加德罗常数的数值,下列说法正确的是 ( )
A.用惰性电极电解500mL饱和食盐水时,若溶液的pH值变为14时,则电极上转移的电子数目为NA。
B.在标准状况下,各为1mol的二氧化硫、三氧化硫的体积均约为22.4L。
C. 在常温常压下,6g石英晶体中,含有0.4NA个硅氧共价键。
D.120g由NaHSO4和KHSO3组成的混合物中含有硫原子NA个。
标准状况下,下列混合气体的平均式量可能是50的是 ( )
A.硫化氢和二氧化硫 B.一氧化氮和氧气
C.二氧化硫和溴化氢 D.碘化氢和氯气
在一个恒容密闭容器中充入11gX气体(摩尔质量为 44g·mol-1),压强为1×105pa。如果保持温度不变,继续充入X气体,使容器内压强达到5×105pa。则此时容器内的气体X的分子数约为 ( )
A.3.3×1025 B.3.3×1024 C.7.5×1023 D.7.5×1022
由二氧化碳、氢气、一氧化碳组成的混合气体在同温、同压下与氮气的密度相同。则该混合气体中二氧化碳、氢气、一氧化碳的体积比为 ( )
A.29∶8∶13 B.22∶1∶14 C.13∶8∶29 D.26∶16∶57
同温、同压下,CO2 和NO的混合气体 20mL,通过足量过氧化钠后气体体积减少到10mL,则原混合气体的体积比可能是 ( )
A.1∶1 B.2∶3 C.3∶2 D.1∶4
乙炔和乙烯的混合气体完全燃烧时,所需氧气的体积是原混合气体的2.7倍,则该混合气体与足量的H2发生加成反应时,消耗H2的体积是原混合气体体积的 ( ) A.1.6倍 B.1.8倍 C.1.4倍 D.1.2倍
在一定条件下,将5体积NO、5体积NO2、6体积O2混合气体置于试管中,并将试管倒立于水槽中,充分反应后,剩余气体的体积是 ( )
A.1体积 B.2体积 C.3体积 4.4体积
19世纪,化学家对氧化锆的化学式有争议.经测定锆的相对原子质量为91,其氯化物蒸气的密度是同溶、同压下H2密度的116-117倍,试判断与氯化物价态相同的氧化锆的化学式 ( )
A.ZrO B.Zr2O C.Zr2O3 D.ZrO2
常温下,向20L真空容器中通入A mol硫化氢和 Bmol氯气(A,B均为不超过5的正整数),反应完全后,容器内气体可能达到的最大密度是 ( )
A.8.5 g·L-1 B.18.25g·L-1 C.18.5 g·L-1 D.35.5 g· L-1
为探究Fe(NO3)2等硝酸盐热分解产物和产物的性质,某化学小组开展如下探究性学习:
【查阅资料】金属活泼性不同,其硝酸盐分解产物不同
(1)K→Na活泼金属的硝酸盐分解生成亚硝酸盐和氧气;
(2)Mg→Cu等较活泼金属的硝酸盐分解生成氧化物、NO2和O2;
(3)Hg以后不活泼金属的硝酸盐分解生成金属、NO2和O2。
2KNO3![]() 2KNO2↑+O2↑ 2Cu(NO3)2
2KNO2↑+O2↑ 2Cu(NO3)2![]() 2CuO+4NO2↑+O2↑
2CuO+4NO2↑+O2↑
2AgNO3![]() 2Ag+2NO2↑+O2↑
2Ag+2NO2↑+O2↑
【实验一】探究Fe(NO3)2热分解固体产物中Fe元素的价态。该小组甲同学将其溶于足量的稀H2SO4得到相应两份溶液,进行以下探究实验。
【提出猜想】
猜想一:Fe元素只显+2价;
猜想二:Fe元素只显______价;
猜想三:Fe元素_________。
【实验操作】①向一份溶液中滴入KSCN溶液;②稀酸性KMnO4溶液中滴入另一份溶液。
【实验现象】实验① ;
实验② 。
【实验结论】猜想二成立,则Fe(NO3)2分解的化学方程式是 。
 【实验二】探究Fe(NO3)2热分解气体产物的性质。小组乙、丙同学进行了如下图所示的实验(收集时操作恰当,几乎没有空气)
【实验二】探究Fe(NO3)2热分解气体产物的性质。小组乙、丙同学进行了如下图所示的实验(收集时操作恰当,几乎没有空气)
实验步骤:①连接仪器;②检查装置气密性;③取一定质量Fe(NO3)2装于大试管,并重新连接好仪器;④加热;⑤……
(1)乙同学使用A装置收集气体,恰好收集到27mL红棕色气体,要从水槽中取出量筒,乙同学的正确操作方法是
。
(2)乙同学用带火星木条检验量筒内气体时,发现木条燃烧,下列判断中正确的是 。
a.气体中只有NO2 b.气体是O2、NO2的混合物
c.支持燃烧的气体只有O2 d.NO2支持燃烧
有机物A、B、C互为同分异构体,分子式均为C5H8O2,有关的转化关系如下图所示。已知:
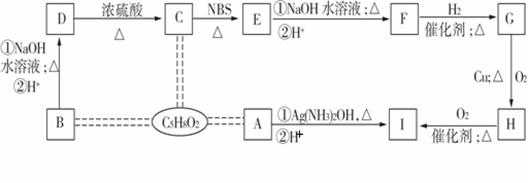
①A
单质Ag;
②B为含有一个五元环的酯;
③CH3—CH===CH—R![]() CH2BrCH===CHR
CH2BrCH===CHR
请回答下列问题:
(1)C中不含氧的官能团的名称是 ,D转化为C的反应类型______________。
(2)B、H的结构简式依次为 、 。
(3)F的加聚反应产物的结构简式为 。
(4)E不能发生反应的反应类型有 (填序号,多选、漏选或错选均不得分)。
①取代反应 ②加成反应 ③银镜反应 ④水解反应 ⑤消去反应 ⑥聚合反应 ⑦氧化反应 ⑧还原反应 ⑨皂化反应 ⑩酯化反应
(5)写出E→F的反应方程式(只写①条件下的反应,有机物用结构简式表示):
。
(6)M是D的同分异构体,且符合以下条件:①分子中只含有一个甲基(—CH3);②能发生银镜反应;③1 mol M与足量Na反应能产生标准状况下22.4 L的气体;④除官能团上的氢原子外,还有两种不同类型的氢原子。请任意写出一种符合条件的M的结构简式:
。
的碳链无支链,且0.1 mol A能与足量Ag(NH3)2OH完全反应可得到43.2 g物质 K Na KCl NaCl
熔点/℃ 63.65 97.8 770 801
沸点/℃ 774 882.9 1500(升华) 1413
根据平衡移动原理分析:
(1)钠能制取钾的原因________________。
(2)该反应的适宜温度是________。
A.97.8~770℃ B.770~774℃
C.774~882.9℃ D.1413~1500℃
金属钾与金属钠的金属性相近,且钾比钠略强。当利用金属钾与钠盐共熔制金属钠时,发现钾与钠的共熔体难以分离。如调整温度到一定程度,则可用金属钠与氯化钾反应制取金属钾。下面是四种物质的熔点、沸点:
物质 K Na KCl NaCl
熔点/℃ 63.65 97.8 770 801
沸点/℃ 774 882.9 1500(升华) 1413
根据平衡移动原理分析:
(1)钠能制取钾的原因________________。
(2)该反应的适宜温度是________。
A.97.8~770℃ B.770~774℃
C.774~882.9℃ D.1413~1500℃
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com