
题目列表(包括答案和解析)
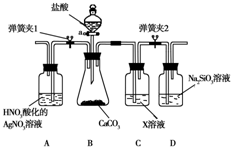 (2012?朝阳区一模)某同学为了验证碳和硅两种元素非金属性的相对强弱,用下图所示装置进行实验(夹持仪器已略去,气密性已检验).
(2012?朝阳区一模)某同学为了验证碳和硅两种元素非金属性的相对强弱,用下图所示装置进行实验(夹持仪器已略去,气密性已检验).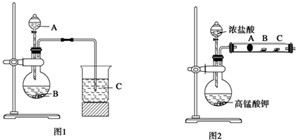
| A、太阳能电池可采用硅材料制作,其应用有利于环保、节能 | B、Na2SiO3可以做木材防火剂 | C、二氧化硅作光导纤维材料 | D、因为高温时二氧化硅与碳酸钠反应放出CO2,所以硅酸的酸性比碳酸强 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com