
题目列表(包括答案和解析)
(1)我国首创以E(单质)—(空气,海水)—石墨(C)电池为能源的新型海水标志灯。该灯以海水为电解质溶液,靠空气中的氧气使E(单质)不断氧化而产生电流。只要把灯放入海水中数分钟,就会发出耀眼的白光,其能量比干电池高20—50倍。该电池的正极反应式是________________________________________________。
(2)将过量气体AF通入AgNO3溶液中得到白色沉淀,将此白色沉淀分成4等份并分别溶于下列物质中:①10 mL水 ②10 mL 0.1 mol·L-1的NaCl溶液 ③10 mL 0.1 mol·L-1的MgCl2溶液 ④10 mL 0.1 mol·L-1的KI溶液。则所得溶液中剩余白色固体质量由大到小的顺序为(填序号)________________________________________________。
(3)已知:
B2(g)+
B2(g)+
试写出BA3与C2反应生成BC2和A
(4)3 mol A的单质与1 mol B的单质在一个体积恒定的密闭容器中反应,生成化合物M,达到平衡时,M的体积分数为m。若将a mol A的单质、b mol B的单质、c mol M同时置于上述容器中,在相同温度下反应,达到平衡时,M的体积分数仍为m,则a、b、c必须满足的关系是____________________________________________________。
 Cu2+(aq)+2OH-(aq), Ksp=2×10-20]
Cu2+(aq)+2OH-(aq), Ksp=2×10-20]  2EC3 (g),△H= -196. 6 kJ mol-1。平衡时容器内气体压强为起始时的90%。
2EC3 (g),△H= -196. 6 kJ mol-1。平衡时容器内气体压强为起始时的90%。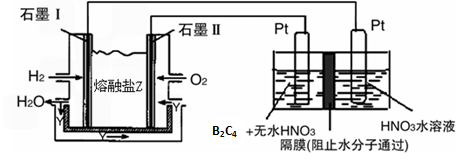
| ||
| ||
 2SO3(g);△H=-196.6KJ?mol-1.平衡时容器内气体压强为起使时的90%.
2SO3(g);△H=-196.6KJ?mol-1.平衡时容器内气体压强为起使时的90%.研究CO2的利用对促进低碳社会的构建具有重要的意义。
(1)将CO2与焦炭作用生成CO,CO可用于炼铁等。
①已知:Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g) ΔH1=+489.0 kJ·mol-1
C(石墨)+CO2(g)=2CO(g) ΔH2=+172.5 kJ·mol-1
则CO还原Fe2O3的热化学方程式为___________________________
②利用燃烧反应可设计成CO/O2燃料电池(以KOH溶液为电解液),写出该电池的负极反应式___________________________________________
(2)某实验将CO2和H2充入一定体积的密闭容器中,在两种不同条件下反应:
CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1
CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1
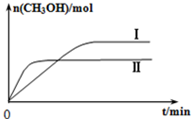
测得CH3OH的物质的量随时间变化如上图所示,回答问题:
①下列措施中能使n(CH3OH)/n(CO2)增大的是________。
| A.升高温度 | B.充入He(g)使体系压强增大 |
| C.将H2O(g)从体系中分离 | D.再充入1 mol CO2和3 mol H2 |
| 容器 | 甲 | 乙 |
| 反应物投入量 | 1 mol CO2、3 mol H2 | a mol CO2、b mol H2、c mol CH3OH(g)、c mol H2O(g) |
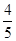 ,要使平衡后乙与甲中相同组分的体积分数相等,且起始时维持反应逆向进行,则c的取值范围为________。
,要使平衡后乙与甲中相同组分的体积分数相等,且起始时维持反应逆向进行,则c的取值范围为________。
 研究CO2的利用对促进低碳社会的构建具有重要的意义.
研究CO2的利用对促进低碳社会的构建具有重要的意义.| c(CH3OH)c(H2O) |
| c(CO2)c3(H2) |
| c(CH3OH)c(H2O) |
| c(CO2)c3(H2) |
| 容 器 | 甲 | 乙 |
| 反应物投入量 | 1molCO2、3molH2 | a molCO2、b molH2、 c molCH3OH(g)、c molH2O(g) |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com