(2011?南京三模)硝基苯酚是合成医药、染料、感光材料的中间体;以苯酚为原料制备硝基苯酚的步骤如下:
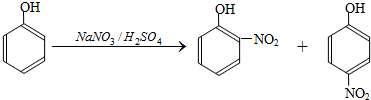
I.在常温下,向250mL三口烧瓶中加试剂(加入的试剂有:A.50mL水;B.17.5gNaNO
3;C.15mL浓硫酸)
Ⅱ.称取4.7g苯酚,与1mL温水混合,并冷却至室温.
Ⅲ.在搅拌下,将苯酚水溶液自滴液漏斗滴入三口烧瓶中,将反应温度维持在20℃左右.
Ⅳ.加完苯酚后,继续搅拌1h,冷却至黑色油状物固化,倾出酸层.然后向油状物中加入20mL水并振摇,先倾出洗液,再用水洗三次,以除净残存的酸.
V.邻硝基苯酚的提纯.固化的黑色油状物主要成分是邻硝基苯酚和对硝基苯酚.
|
密度
(g?mL-1) |
熔点
(℃) |
沸点
(℃) |
溶解性 |
其他 |
| 邻硝基苯酚 |
1.495 |
44.45 |
214 |
微溶于冷水,易溶于热水 |
能与水蒸气一同挥发 |
| 对硝基苯酚 |
11.481 |
113.4 |
279 |
稍溶于水 |
不与水蒸气一同挥发 |
(1)步骤I中加入试剂的先后顺序为
ACB
ACB
(填序号)
(2)苯酚有腐蚀性,步骤Ⅱ中若不慎使苯酚触及皮肤,应
立刻用酒精棉擦洗
立刻用酒精棉擦洗
.苯酚中加少许水可降低熔点,使其中室温下即呈液态,这样操作的作用是
便于滴加,同时也可以加快反应
便于滴加,同时也可以加快反应
.
(3)步骤Ⅲ中,将反应温度维持在20℃左右的原因是
当温度过高,一元硝基酚有可能发生进步硝化,当温度偏低,又将减缓反应速度
当温度过高,一元硝基酚有可能发生进步硝化,当温度偏低,又将减缓反应速度
.
(4)步骤Ⅳ中,若黑色油状物未固化,则可用
分液漏斗
分液漏斗
(填实验仪器)将黑色油状物分出.
(5)根据题给信息,不使用温度计,设计步骤V得到纯净的邻硝基苯酚的实验方案;
将油状混合物与水混合加热蒸馏,将馏出液冷却过滤,收集晶体,即得邻硝基苯酚产物
将油状混合物与水混合加热蒸馏,将馏出液冷却过滤,收集晶体,即得邻硝基苯酚产物
.


