
化学兴趣小组的同学对碳及碳的氧化物进行了一系列拓展性探究学习.
【探究一】二氧化碳的性质的拓展探究
(1)倾倒二氧化碳实验
甲、乙两同学将两瓶完全相同的足够的二氧化碳气体,分别以甲图、乙图的方式将二氧化碳气体慢慢倒入烧杯中,请分析回答:
①甲同学用甲图的方式倾倒,观察到两根蜡烛是由下而上熄灭,该实验说明二氧化碳具有
既不能燃烧也不能支持燃烧
既不能燃烧也不能支持燃烧
、
密度比空气大
密度比空气大
的性质.
②乙同学用乙图的方式倾倒,观察到的结果是两根蜡烛都没有熄灭,请你联系学科知识分析,蜡烛没有熄灭的原因
二氧化碳受热后密度变得比空气小,随着热气流上升,因此二氧化碳没有进入烧杯
二氧化碳受热后密度变得比空气小,随着热气流上升,因此二氧化碳没有进入烧杯
.
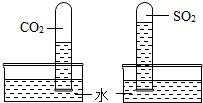
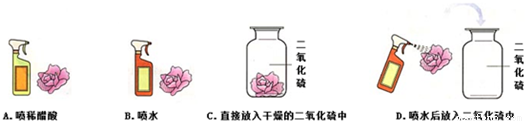
(2)二氧化碳与二氧化硫溶解性对比实验
丙同学用相同的试管分别收集了二氧化碳和二氧化硫,做了如右图所示的对比实验,现象如图.分析该现象得到的结论是
二氧化硫在水中的溶解能力大于二氧化碳
二氧化硫在水中的溶解能力大于二氧化碳
.该实验设计的思路:一是利用对比实验,二是利用
气体溶于水使试管内压强减小
气体溶于水使试管内压强减小
的原理产生实验现象.
【探究二】在学习了木炭还原氧化铜的实验后,小明对课本上实验进行如下改进:
将CuO和足量炭粉充分混合,平铺在反应管a中,在b瓶中盛足量澄清石灰水,按图连接仪器(加热装置和固定装置省略,下同).
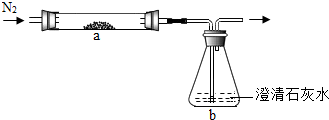
实验开始时缓慢通入氮气,过一段时间后,加热反应管a,观察到管内有红色固体产生,b瓶的溶液中出现白色浑浊.待反应完全后,停止加热,仍继续通氮气,直至反应管冷却.根据以上叙述回答问题:
(1)通N
2的目的是
将反应管内的空气(或O2)排尽
将反应管内的空气(或O2)排尽
.
(2)写出b瓶中发生反应的化学方程式
CO2+Ca(OH)2═CaCO3↓+H2O
CO2+Ca(OH)2═CaCO3↓+H2O
.
(3)停止加热前是否需要先断开a和b的连接处?
不需要
不需要
.为什么?
因为继续通入氮气,b瓶中的液体不会倒吸入a管
因为继续通入氮气,b瓶中的液体不会倒吸入a管
.
(4)小梅认为:木炭与氧化铜反应产生的气体中既有CO
2,又有CO.为验证此猜想,小梅对上述装置做了如下改进并实验:

小梅观察到
甲中有红色固体生成
甲中有红色固体生成
现象,证明了气体中的确含有CO.
小明认为小梅的实验不能证明木炭与氧化铜反应产生了CO
2,其理由是
因为甲中CO与CuO反应生成了CO2也使澄清石灰水变浑浊,因此不能证明木炭与氧化铜反应生成了CO2
因为甲中CO与CuO反应生成了CO2也使澄清石灰水变浑浊,因此不能证明木炭与氧化铜反应生成了CO2
.(5)本实验的尾气是否需处理?如需处理,请回答如何处理;如不需处理,请说明理由:
需要,因为反应过程中有CO产生,可在尾气管口放上一个点燃的酒精灯
需要,因为反应过程中有CO产生,可在尾气管口放上一个点燃的酒精灯
.

 化学兴趣小组的同学对碳及碳的氧化物进行了一系列拓展性探究学习.
化学兴趣小组的同学对碳及碳的氧化物进行了一系列拓展性探究学习.



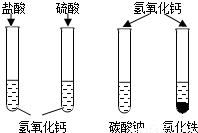
 (2012?衢州)学习碱的性质时,同学们在实验室中做“检测氢氧化钙性质”的实验,实验方案如图所示(说明:实验中使用的药品均是溶液).请回答下列问题:
(2012?衢州)学习碱的性质时,同学们在实验室中做“检测氢氧化钙性质”的实验,实验方案如图所示(说明:实验中使用的药品均是溶液).请回答下列问题: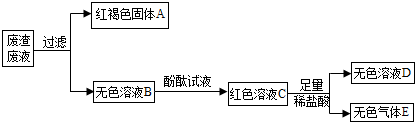
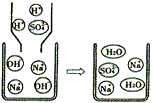 氢氧化钠俗名苛性钠,是一种重要的化工原料.下列研究从其结构、制备方法、性质以及变化规律等角度进行,请根据要求回答相应问题.
氢氧化钠俗名苛性钠,是一种重要的化工原料.下列研究从其结构、制备方法、性质以及变化规律等角度进行,请根据要求回答相应问题.