碘被称为“智力元素”,科学合理地补充碘可防止碘缺乏病.碘酸钾(KIO
3)是国家规定的食盐加碘剂,它的晶体为白色,可溶于水.碘酸钾在酸性介质中与碘化物作用生成单质碘.
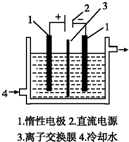
(1)以碘为原料,通过电解制备碘酸钾的实验装置如图所示.电解前,先将一定量的精制碘溶于过量氢氧化钾溶液,溶解时发生反应:3I
2+6KOH═5KI+KIO
3+3H
2O,将该溶液加入阳极区.另将氢氧化钾溶液加入阴极区,电解槽用水冷却.电解时,阳极上发生反应的电极反应式为
;每生成1mol KIO
3,电路中通过电子的物质的量是
mol;
(2)若用不同种电池作为上述实验的电源,请分析电池反应.
①铅蓄电池总反应的化学方程式为:Pb+PbO
2+2H
2SO
42H
2O+2PbSO
4,则它在充电时的阳极反应为:
;
②MnO
2-Zn组成碱性干电池在放电时的负极反应为:
;
③以丙烷为燃料制作新型燃料电池,电池的正极通入O
2和CO
2,负极通入丙烷,电解质是熔融碳酸盐,电池总反应方程式为:C
3H
8+5O
2═3CO
2+4H
2O.写出该电池正极的电极反应:
;
④当产生相同质量的KIO
3时,理论上,上述三种电池中分别消耗的Pb、Zn、丙烷的物质的量之比是
;
(3)电解过程中,为确定电解是否完成,需检验电解液中是否有I
-.请设计一个检验电解液中是否有I
-的实验方案.(写出实验方法、现象和结论)

 (1)二甲醚燃料电池的正极反应式为
(1)二甲醚燃料电池的正极反应式为 碘被称为“智力元素”,科学合理地补充碘可防止碘缺乏病.碘酸钾(KIO3)是国家规定的食盐加碘剂,它的晶体为白色,可溶于水.碘酸钾在酸性介质中与碘化物作用生成单质碘.
碘被称为“智力元素”,科学合理地补充碘可防止碘缺乏病.碘酸钾(KIO3)是国家规定的食盐加碘剂,它的晶体为白色,可溶于水.碘酸钾在酸性介质中与碘化物作用生成单质碘.