A、D、E、M、L是原子序数依次增大的五种短周期元素.已知A是元素周期表中原子半径最小的元素;D的某种单质是天然存在的最硬物质;E是地壳中含量最多的元素;M与A位于同一主族;L与M能够形成ML型离子化合物.回答下列问题:
(1)元素D在元素周期表中的位置是
第二周期第IVA族
第二周期第IVA族
.
(2)L的单质与M的最高价氧化物对应水化物反应的离子方程式为
Cl2+2OH-=ClO-+Cl-+H2O
Cl2+2OH-=ClO-+Cl-+H2O
.
(3)25℃时,物质的量浓度相同的MEA、MADE
3、MLE三种溶液,水的电离程度由大到小的顺序为
NaClO>NaHCO3>NaOH
NaClO>NaHCO3>NaOH
.(填化学式)
(4)设化合物甲、乙、丙分别为DA
3EA、DA
3EDA
3、A
2E.
ⅰ:已知:(1)丙(g)═丙(l)△H=-Q
1 kJ?mol
-1(2)2甲(l)+3E
2(g)═2DE
2(g)+4丙(g)△H=-Q
2 kJ?mol
-1Q
1、Q
2均大于0.若要使32g液态甲完全燃烧并恢复到室温,放出的热量为
(2Q1+0.5Q2)kJ
(2Q1+0.5Q2)kJ
.
ⅱ:已知:2甲(g)=乙(g)+丙(g).在某温度下,在1L密闭容器中加入甲,反应到10分钟时达到平衡,此时测得各组分的浓度如下:
| 物 质 |
甲 |
乙 |
丙 |
| 浓度/mol?L-1 |
0.01 |
0.2 |
0.2 |
①该温度下反应的平衡常数为
400
400
.
②10min内平均反应速率v(甲)=
0.04mol?L-1?min-1
0.04mol?L-1?min-1
.
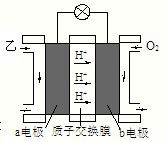
ⅲ:如图是乙为燃料的绿色电源工作原理示意图.若b电极的反应式为:3O
2+12e
-+12H
+═6H
2O,则a电极的反应式为:
(CH3)2O-12e-+3H2O=2CO2+12H+
(CH3)2O-12e-+3H2O=2CO2+12H+
.