
题目列表(包括答案和解析)
(1)2Fe3++2I-====2Fe2++I2
(2)2Fe2++Br2====2Fe3++2Br-
(3)2Br-+Cl2====2Cl-+Br2
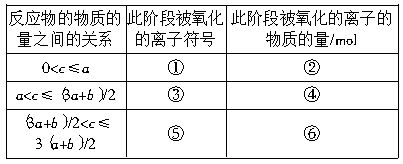
现有某混合溶液中含amolFeI2和bmolFeBr2,向该混合液中逐渐通入cmolCl2,试根据以上化学原理分析,确定当下列物质的量的离子被氧化时,通入Cl2的物质的量的取值范围:
(1)当只有I-被氧化时,c的取值范围为多少?
(2)当有Fe2+被氧化时,c的取值范围为多少?
(3)当有Br-被部分氧化时,c的取值范围是多少?
| ||
| ||
| ||
| ||
| ||
化学方程式可简明地体现元素及其化合物的性质。已知:
氧化还原反应:2FeCl3 + 2HI = 2FeCl2+ I2 + 2HCl;
2Co(OH)3 + 6HCl = 2CoCl2 + Cl2↑ + 6H2O
2FeCl2 + Cl2 = 2FeCl3
复分解反应: 2CH3COOH + K2CO3 = 2CH3COOK+ CO2 ↑ + H2O;
KCN + CO2 + H2O = HCN + KHCO3
热分解反应: 4NaClO △3NaCl + NaClO4;
NaClO4 △NaCl + 2O2↑
下列说法不正确是( )
A.氧化性(酸性溶液):Co(OH)3 >FeCl3 > I2
B.还原性(酸性溶液):FeCl2 > HI > HCl
C.酸性(水溶液):CH3COOH >H2CO3 >HCN
D.热稳定性:NaCl>NaClO4>NaClO
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com