
题目列表(包括答案和解析)
【化学--选修2化学与技术】(15分)
高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。其生产工艺如下: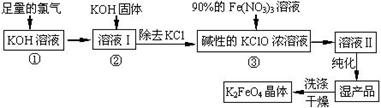
已知:2KOH + Cl2 ═ KCl + KClO + H2O(条件:温度较低)
6KOH + 3Cl2 ═ 5KCl + KClO3 + 3H2O(条件:温度较高)
回答下列问题:
(1)该生产工艺反应①应在 (填“温度较高”或“温度较低”)的情况下进行;
(2)写出工业上制取Cl2的化学方程式 ;
(3)K2FeO4具有强氧化性的原因 ;
(4)配制KOH溶液时,是在每100 mL水中溶解61.6 g KOH固体( 该溶液的密度为1.47 g/mL),它
的物质的量浓度为 ;
(5)在“溶液I”中加KOH固体的目的是 :
| A.与 “溶液I” 中过量的Cl2继续反应,生成更多的KClO |
| B.KOH固体溶解时会放出较多的热量,有利于提高反应速率 |
| C.为下一步反应提供反应物 |
| D.使副产物KClO3转化为 KClO |
在反应3Cl2+6KOH(浓)![]() KClO3+5KCl+3H2O中,氧化剂与还原剂物质的量之比为
KClO3+5KCl+3H2O中,氧化剂与还原剂物质的量之比为
A. 1:5 B. 4:1 C. 5:1 D. 1:4
在反应3Cl2+6KOH(浓)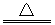 KClO3+5KCl+3H2O中,氧化剂与还原剂物质的量之比为
KClO3+5KCl+3H2O中,氧化剂与还原剂物质的量之比为
A. 1:5 B. 4:1 C. 5:1 D. 1:4
(12分)、高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。其生产工艺如下:
已知:① 2KOH + Cl2 → KCl + KClO + H2O(条件:温度较低)
② 6KOH + 3Cl2 → 5KCl + KClO3+ 3H2O(条件:温度较高)
③ 2Fe(NO3)3 + 2KClO + 10KOH→ 2K2FeO4 + 6KNO3 + 3KCl + 5H2O
回答下列问题:
⑴该生产工艺应在 __ (填“温度较高”或“温度较低”)的情况下进行;
⑵写出工业上制取Cl2的化学方程式 __ ;
⑶配制KOH溶液时,是在每100 mL水中溶解61.6 g KOH固体(该溶液的密度为1.47 g/mL),它的物质的量浓度为 __ ;
⑷在“反应液I”中加KOH固体的目的是 __ :
A.与“反应液I”中过量的Cl2继续反应,生成更多的KClO
B.KOH固体溶解时会放出较多的热量,有利于提高反应速率
C.为下一步反应提供反应物 D.使副产物KClO3转化为 KClO
⑸从“反应液II”中分离出K2FeO4后,会有副产品 _ (写化学式),它们都是重要的化工产品,具体说出其中一种物质的用途 _ 。
(12分)、高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。其生产工艺如下:

已知:① 2KOH + Cl2 → KCl + KClO + H2O(条件:温度较低)
② 6KOH + 3Cl2 → 5KCl + KClO3 + 3H2O(条件:温度较高)
③ 2Fe(NO3)3 + 2KClO + 10KOH → 2K2FeO4 + 6KNO3 + 3KCl + 5H2O
回答下列问题:
⑴该生产工艺应在 __ (填“温度较高”或“温度较低”)的情况下进行;
⑵写出工业上制取Cl2的化学方程式 __ ;
⑶配制KOH溶液时,是在每100 mL水中溶解61.6 g KOH固体(该溶液的密度为1.47 g/mL),它的物质的量浓度为 __ ;
⑷在“反应液I”中加KOH固体的目的是 __ :
A.与“反应液I”中过量的Cl2继续反应,生成更多的KClO
B.KOH固体溶解时会放出较多的热量,有利于提高反应速率
C.为下一步反应提供反应物 D.使副产物KClO3转化为 KClO
⑸从“反应液II”中分离出K2FeO4后,会有副产品 _ (写化学式),它们都是重要的化工产品,具体说出其中一种物质的用途 _ 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com