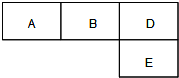
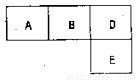
有M、A、B、D、N、E五种短周期元素,原子序数依次增大.M元素的单质是自然界最轻
的气体,N元素的原子半径是所在周期原子半径最大的.A、B、D、E分别在右表(周期表的一部分)占有相应的位置,它们的原子序数之和为37.试回答:
(1)A、B、D、E四种元素分别与M元素形成的简单化合物中,沸点最高的是
H2O
H2O
(填化学式).
(2)M、D、E、N形成的简单离子的半径由大到小的关系是(写离子符号)
S2->O2->Na+>H+
S2->O2->Na+>H+
.
(3)A、B、D、M可组成多种18电子分子,请写出1种具有18电子的有机物的分子式
CH3OH
CH3OH
.
(4)由A、D、N三种元素组成的无机物,其水溶液呈碱性,用离子方程式表示其原因
CO32-+H2O?HCO3-+OH-
CO32-+H2O?HCO3-+OH-
.
(5)元素B的氢化物与元素D单质在一定条件下发生置换反应,在该反应中氧化剂与还原剂的物质的量之比为
3:4
3:4
.
(6)在由M、D、N、E四种元素构成的化合物的水溶液中滴入少量的Ba(OH)
2溶液,写出可能发生的所有反应的离子方程式
2H++2OH-+SO42-+Ba2+═BaSO4↓+2H2O或2HSO3-+2OH-+Ba2+═BaSO3↓+2H2O+SO32-
2H++2OH-+SO42-+Ba2+═BaSO4↓+2H2O或2HSO3-+2OH-+Ba2+═BaSO3↓+2H2O+SO32-
.

 有M、A、B、D、N、E五种短周期元素,原子序数依次增大.M元素的单质是自然界最轻
有M、A、B、D、N、E五种短周期元素,原子序数依次增大.M元素的单质是自然界最轻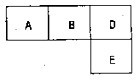 有M、A、B、D、N、E五种短周期元素,原子序数依次增大.M元素的单质是自然界最轻的气体,N元素的原子半径是所在周期原子半径最大的.A、B、D、E分别在表(周期表的一部分)占有相应的位置,它们的原子序数之和为37.试回答:
有M、A、B、D、N、E五种短周期元素,原子序数依次增大.M元素的单质是自然界最轻的气体,N元素的原子半径是所在周期原子半径最大的.A、B、D、E分别在表(周期表的一部分)占有相应的位置,它们的原子序数之和为37.试回答: