
题目列表(包括答案和解析)
(13分)A、B、C、D、E、X、Y为中学常见的七种物质,它们有如下转化关系(部分产物与反应条件略去):
(1)若A为金属单质,B为氢气,X为盐酸,Y为易溶强碱溶液。则A物质的名称是 ;D与Y反应的离子方程式为;
(2)若A为固体非金属单质,B为水,X为强酸,Y为含钠元素的化合物。则A物质的名称可能是 ;D与Y反应的离子方程式为可能为
;
(3)若A、C为同主族元素组成的单质,通常状况下,A为气体,C为液体,Y为金属单质。则D溶液显 (填酸或碱)性,原因是
(用离子方程式作答)
将NaOH溶液加入E的溶液中,可观察到的现象是 ;
D→E的化学反应方程式为 。
【解析】(1)根据图中的转化特点可知,C和强碱反应生成物D还能溶解在强碱中,常见的是铝的化合物的转化,再结合A是金属可知,A是铝和盐酸的÷生成氢气和氯化铝,所以D是氢氧化铝,E是偏铝酸钠。
(2)常见非金属单质能和酸反应生成水的,一般强氧化性酸和C或S反应,生成的CO2或SO2可与氢氧化钠反应生成正盐或酸式盐。
(3)常见的液体单质是溴,A能置换出溴,说明A是氯气。根据转化特点可判断,Y是变价的金属铁。铁离子在溶液中存在水解平衡,溶液显酸性。
(13分)A、B、C、D、E、X、Y为中学常见的七种物质,它们有如下转化关系(部分产物与反应条件略去):
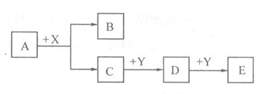
(1)若A为金属单质,B为氢气,X为盐酸,Y为易溶强碱溶液。则A物质的名称是 ;D与Y反应的离子方程式为;
(2)若A为固体非金属单质,B为水,X为强酸,Y为含钠元素的化合物。则A物质的名称可能是 ;D与Y反应的离子方程式为可能为
;
(3)若A、C为同主族元素组成的单质,通常状况下,A为气体,C为液体,Y为金属单质。则D溶液显 (填酸或碱)性,原因是
(用离子方程式作答)
将NaOH溶液加入E的溶液中,可观察到的现象是 ;
D→E的化学反应方程式为 。
【解析】(1)根据图中的转化特点可知,C和强碱反应生成物D还能溶解在强碱中,常见的是铝的化合物的转化,再结合A是金属可知,A是铝和盐酸的÷生成氢气和氯化铝,所以D是氢氧化铝,E是偏铝酸钠。
(2)常见非金属单质能和酸反应生成水的,一般强氧化性酸和C或S反应,生成的CO2或SO2可与氢氧化钠反应生成正盐或酸式盐。
(3)常见的液体单质是溴,A能置换出溴,说明A是氯气。根据转化特点可判断,Y是变价的金属铁。铁离子在溶液中存在水解平衡,溶液显酸性。
A、B、C、D是常见的短周期元素,根据有关信息,按要求回答问题:
信息①:A、B、C、D原子序数依次增大,且原子核外最外层电子数均不少于2;
(1)根据信息①:A一定不是????????? (填序号);
A.氢????? B. 碳????? C.氧?????? D.硫
信息②:上述四种元素的单质常温下均为固体,其最高价氧化物中有两种能溶于稀硫酸,三种能溶于浓氢氧化钠溶液;
(2)这四种元素中是否可能有一种是铝元素????????? (填“可能”或“不可能”);
信息③:A与D同主族,工业上常用A高温下还原DO2制取D;
(3)A与DO2反应的化学方程式为???????????????????????????????? ;
信息④:向上述四种元素的单质组成的混合物中加入足量盐酸溶液,固体部分溶解,过滤后向滤液中加入过量的烧碱溶液,最终溶液中析出白色沉淀;
(4)白色沉淀物的化学式为???????????? 。
A、B、C、D是常见的短周期元素,根据有关信息,按要求回答问题:
信息①:A、B、C、D原子序数依次增大,且原子核外最外层电子数均不少于2;
(1)根据信息①:A一定不是 (填序号);
A.氢 B. 碳 C.氧 D.硫
信息②:上述四种元素的单质常温下均为固体,其最高价氧化物中有两种能溶于稀硫酸,三种能溶于浓氢氧化钠溶液;
(2)这四种元素中是否可能有一种是铝元素 (填“可能”或“不可能”);
信息③:A与D同主族,工业上常用A高温下还原DO2制取D;
(3)A与DO2反应的化学方程式为 ;
信息④:向上述四种元素的单质组成的混合物中加入足量盐酸溶液,固体部分溶解,过滤后向滤液中加入过量的烧碱溶液,最终溶液中析出白色沉淀;
(4)白色沉淀物的化学式为 。

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com