
МвДҝБРұн(°ьАЁҙр°ёәНҪвОц)
(8·Ц)ЗлСЎФсәПКК·Ҫ·ЁөДЧЦДёҙъәЕМоҝХЈә
(1)ҙУГәҪ№УНЦРМбИЎ¶юјЧұҪ________Ј»
(2)ҙУәЈЛ®ЦРМбИЎҙЦСО________Ј»
(3)К®БщНйЧӘұдОӘРБНйәНРБП©________Ј»
(4)ЗбІсУНЧӘұдОӘТТП©ЎўұыП©өИІ»ұҘәНМю________Ј»
(5)ГәЧӘ»ҜОӘҪ№МҝЎўГәҪ№УНөИ________Ј»
(6)№ӨТөЙПУЙСх»ҜВБЦЖИЎҪрКфВБ________Ј»
(7)ҙУМъҝуКҜЦРМбИЎҪрКфМъ________Ј»
(8)МбҙҝЗвСх»ҜМъҪәМе(іэИҘЖдЦРөДФУЦКАлЧУ)________ЎЈ
AЈ®№эВЛЎЎBЈ®БСҪвЎЎCЈ®·ЦБуЎЎDЈ®БС»ҜЎЎEЈ®ёЙБуЎЎFЈ®»№ФӯЎЎGЈ®өзҪвЎЎHЈ®ИЬҪвЎЎ
IЈ®ЙшОцЎЎJЈ®Хф·ўЎЎKЈ®Сх»Ҝ
(ГҝҝХ3·Ц№ІјЖ10·ЦЈ©БтЛб№ӨТөЦР·ПФьіЖОӘБтЛбФьЈ¬ЖдіЙ·ЦОӘSiO2ЎўFe2O3ЎўAl2O3ЎўMgOЎЈДіМҪҫҝРФС§П°РЎЧйөДН¬С§ЙијЖТФПВ·Ҫ°ёЈ¬ҪшРРБтЛбФьЦРҪрКфФӘЛШөДМбИЎКөСйЎЈ
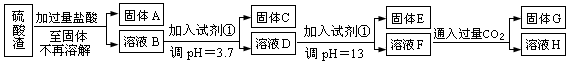
ТСЦӘИЬТәpH=3.7КұЈ¬Fe3+ТСҫӯіБөнНкИ«Ј»Т»Л®әП°ұөзАліЈКэKb=1.8ЎБ10Јӯ5Ј¬ЖдұҘәНИЬТәЦРc(OHЈӯ)ФјОӘ1ЎБ10-3molЎӨL-1ЎЈЗл»ШҙрЈә
ЈЁ1Ј©РҙіцAУлЗвСх»ҜДЖИЬТә·ҙУҰөД»ҜС§·ҪіМКҪЈә ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЈ
ЈЁ2Ј©ЙПКцБчіМЦРБҪҙОК№УГКФјБўЩЈ¬НЖІвКФјБўЩУҰёГКЗ ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЈЁМоТФПВЧЦДёұаәЕЈ©
AЈ®ЗвСх»ҜДЖЎЎЎЎЎЎЎЎЎЎЎЎ BЈ®Сх»ҜВБЎЎЎЎЎЎЎЎЎЎЎЎ ЎЎЎЎ CЈ®°ұЛ®ЎЎЎЎЎЎЎЎЎЎЎЎ ЎЎDЈ®Л®
ЈЁ3Ј©ИЬТәDөҪ№ММеE№эіМЦРРиТӘҝШЦЖИЬТәpH=13Ј¬Из№ыpH№эРЎЈ¬ҝЙДЬөјЦВөДәу№ыКЗЎЎЎЎЎЎЎЎЎЎЎЎ Ј»ЈЁИОРҙТ»өгЈ©
ЈЁ4Ј©HЦРИЬЦКөД»ҜС§КҪЈәЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ Ј»
ЈЁ5Ј©јЖЛгИЬТәFЦРc(Mg2+)ЈҪЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЈЁ25ЎжКұЈ¬ЗвСх»ҜГҫөДKsp=5.6ЎБ10-12Ј©
 ПВНјЛщКҫЈЁ·ҙУҰМхјюҫщТСВФИҘЈ©Ј®
ПВНјЛщКҫЈЁ·ҙУҰМхјюҫщТСВФИҘЈ©Ј®
| ||
| Ўч |
| ||
| Ўч |

| X-Y | X=Y | XЎФY | |
| BDөДјьДЬЈЁkJ?mol-1Ј© | 357.7 | 798.9 | 1071.9 |
| C2өДјьДЬЈЁkJ?mol-1Ј© | 154.8 | 418.4 | 941.7 |
AЎўBЎўCЎўDКЗ¶МЦЬЖЪФӘЛШРОіЙөДЛДЦЦЖшМеөҘЦКЎЈEЎўFҫщОӘЖшМеЈ¬ЗТFОӘәмЧШЙ«ЎЈУР№ШөДЧӘ»Ҝ№ШПөИзПВНјЛщКҫЈЁ·ҙУҰМхјюҫщТСВФИҘЈ©ЎЈ

Зл»ШҙрПВБРОКМвЈә
ЈЁ1Ј©DөД»ҜС§КҪОӘ Ј»
ЈЁ2Ј©·ҙУҰўЫөДАлЧУ·ҪіМКҪОӘ ЎЈ
ЈЁ3Ј©YәНEФЪТ»¶ЁМхјюПВҝЙ·ҙУҰЙъіЙBәНZЈ¬ХвКЗТ»ёцҫЯУРКөјКТвТеөД·ҙУҰЈ¬ҝЙПыіэE¶Ф»·ҫіөДОЫИҫЈ¬ёГ·ҙУҰөД»ҜС§·ҪіМКҪОӘ ЎЈ
ЈЁ4Ј©0.1mol/LөДXИЬТәәН0.1mol/LөДYИЬТәөИМе»э»мәПЈ¬ИЬТәіК________РФЈ»ЈЁМоЎ°ЛбЎұЎўЎ°јоЎұ»тЎ°ЦРЎұЈ©ёГИЬТәЦРёчАлЧУЕЁ¶ИҙуРЎ№ШПөОӘЈә_______________________
ЈЁ5Ј©іЈОВПВ0.1mol/LөДYИЬТәЦРc(H+)/c(OH-)=110Јӯ8Ј¬ПВБРРрКцХэИ·өДКЗЈЁ Ј©
AЈ®ёГИЬТәөДpH=11Ј»
BЈ®ёГИЬТәЦРөДИЬЦКөзАліцөДСфАлЧУЕЁ¶И0.1mol/L
CЈ®ёГИЬТәЦРЛ®өзАліцөДc(H+)Улc(OH-)іЛ»эОӘ110Јӯ22
DЈ® pH=3өДСОЛбИЬТәV1 LУлёГ0.1mol/LөДYИЬТәV2 L»мәП,Иф»мәПИЬТәpH=7Ј¬Фт:V1>V2
EЈ®Ҫ«pH=11өДYИЬТәјУЛ®ПЎКН100ұ¶әуЈ¬pHЦөОӘ9Ј»
ЈЁ6Ј©»ҜәПОпEФЪТ»¶ЁМхјюПВУЪТ»¶ЁМе»эөДИЭЖчЦРҝЙ·ўЙъЙнСх»Ҝ»№Фӯ·ҙУҰЈ¬ІвөГИЭЖчДЪЖшМеөДС№ЗҝВФРЎУЪФӯАҙөД2/3Ј¬ЗлРҙіцёГ·ҙУҰөД»ҜС§·ҪіМКҪ
°Щ¶ИЦВРЕ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com