
题目列表(包括答案和解析)
铁元素是重要的金属元素,单质铁在工业和生活中使用得最为广泛。铁还有很多重要的化合物及其化学反应。如铁与水反应:3Fe(s)+4H2O(g)=Fe3O4(s)+4H2(g) △H
(1)上述反应的平衡常数表达式K=_______。
(2) 已知:①3Fe(s)+2O2(g)=Fe3O4(s) △H1=-1118.4kJ/mol
②2H2(g)+O2(g)=2H2O(g) △H2=-483.8kJ/mol
③2H2(g)+O2(g)=2H2O(l) △H3=-571.8kJ/mol
则△H=_______。
(3)在t0C时,该反应的平衡常数K=16,在2L恒温恒容密闭容器甲和乙中,分别按下表所示加入物质,反应经过一段时间后达到平衡。
|
|
Fe |
H2O(g) |
Fe3O4 |
H2 |
|
甲/mol |
1.0 |
1.0 |
1.0 |
1.0 |
|
乙/mol |
1.0 |
1.5 |
1.0 |
1.0 |
①甲容器中H2O的平衡转化率为_______ (结果保留一位小数)。
②下列说法正确的是_______ (填编号)
A.若容器压强恒定,则反应达到平衡状态
B.若容器内气体密度恒定,则反应达到平衡状态
C.甲容器中H2O的平衡转化率大于乙容器中H2O的平衡转化率
D.增加Fe3O4就能提高H2O的转化率
(4)若将(3)中装置改为恒容绝热(不与外界交换能量)装置,按下表充入起始物质,起始时与平衡后的各物质的量见表:
|
|
Fe |
H2O(g) |
Fe3O4 |
H2 |
|
起始/mol |
3.0 |
4.0 |
0 |
0 |
|
平衡/mol |
m |
n |
p |
q |
若在达平衡后的装置中继续加入A、B、C三种状况下的各物质,见表:
|
|
Fe |
H2O(g) |
Fe3O4 |
H2 |
|
A/mol |
3.0 |
4.0 |
0 |
0 |
|
B/mol |
0 |
0 |
1 |
4 |
|
C/mol |
m |
n |
p |
q |
当上述可逆反应再一次达到平衡状态后,上述各装置中H2的百分含量按由大到小的顺序排列的关系是
________(用A、B、C表示)。
(5)已知Fe(OH)3的Ksp=2.79×10-39,而FeCl3溶液总是显示较强的酸性,若某FeCl3溶液的pH为3,则该溶液中c(Fe3+)=________mol • L-1 (结果保留3位有效数字)
利用天然气合成氨的工艺流程示意图如下:
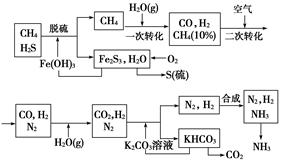
依据上述流程,完成下列填空:
(1)n mol CH4经一次转化后产生CO 0.9n mol,产生H2________mol(用含n的代数式表示)。
(2)K2CO3溶液和CO2反应在加压条件下进行,加压的理论依据是________(填字母代号)。
a.相似相溶原理 b.平衡移动原理 c.酸碱中和原理
(3)由KHCO3分解得到的CO2可以用于________(写出CO2的一种重要用途)。
(4)整个流程有三处循环,一是Fe(OH)3循环,二是K2CO3溶液循环,三是________循环。
(15分)
1-1 2011年是国际化学年,是居里夫人获得诺贝尔化学奖100周年。居里夫人发现的两种化学元素的元素符号和中文名称分别是 和 。
1-2 向TiOSO4水溶液中加入锌粒,反应后溶液变为紫色。在清夜中滴加适量的CuCl2水溶液,产生白色沉淀。生成白色沉淀的离子方程式是 ;继续滴加CuCl2水溶液,白色沉淀消失,其离子方程式是 。
1-3 20世纪60年代维也纳大学V.Gutmann研究小组报道,三原子分子A可由SF4和NH3反应合成;A被AgF2氧化得到沸点为为27℃的三元化合物B。A和B分子中的中心原子与同种端位原子的核间距几乎相等;B分子有一根三种轴和3个镜面。画出A和B的结构式(明确示出单键和重键,不在纸面上的键用楔形键表示,非键合电子不必标出)。
1-4 画出Al2(n-C4H9)4H2和Mg[Al(CH3)4]2的结构简式。
1-5 已知EӨ(FeO42—/Fe3+) = 2.20V,EӨ(FeO42—/Fe(OH)3) =0.72 V。
① 写出氯气和三氯化铁反应形成高铁酸根的离子方程式。 。
② 写出高铁酸钾在酸性水溶液中分解的离子方程式。 。
③ 用高铁酸钾与镁等组成碱性电池,写出该电池的电极反应 。

依据上述流程,完成下列填空。
(1)天然气脱硫时的化学方程式是________________。
(2)nmol CH4经一次转化后产生CO0.9nmol,产生H2________mol。(用含n的代数式表示)
(3)K2CO3(aq)和CO2反应在加压下进行,加压的理论依据是__________。(多选扣分)
a.相似相溶原理
b.勒夏特列原理
c.酸碱中和原理
(4)由KHCO3分解得到的CO2可以用于__________ (写出CO2的一种重要用途)。
(5)整个流程有三处循环,一是Fe(OH)3循环,二是K2CO3(aq)循环,请在上述流程图中标出第三处循环(循环方向、循环物质)。
镍电池广泛应用于混合动力汽车系统,电极材料由Ni(OH)2、碳粉、氧化铁等涂覆在铝箔上制成。由于电池使用后电极材料对环境有危害。某兴趣小组对该电池电极材料进行资源回收研究,设计实验流程如下:
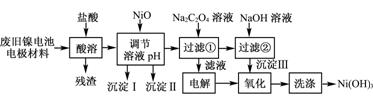
已知:①NiCl2易溶于水,Fe3+不能氧化Ni2+。
②已知实验温度时的溶解度:NiC2O4>NiC2O4·H2O>NiC2O4·2H2O
③某温度下一些金属氢氧化物的Ksp及沉淀析出的理论pH如下表所示:
|
M(OH)n |
Ksp |
|
|
|
pH |
|
|
|
|
开始沉淀 |
沉淀完全 |
|
|
|
Al(OH)3 |
1.9×10-23 |
3.4 |
4.2 |
|
Fe(OH)3 |
3.8×10-38 |
2.5 |
2.9 |
|
Ni(OH)2 |
1.6×10-14 |
7.6 |
9.8 |
回答下列问题:
(1) 用NiO调节溶液的pH,依次析出沉淀Ⅰ________和沉淀Ⅱ__________(填化学式)。
(2) 写出加入Na2C2O4溶液的反应的化学方程式: 。
(3) 检验电解滤液时阳极产生的气体的方法: 。
(4) 写出“氧化”反应的离子方程式: 。
(5) 如何检验Ni(OH)3已洗涤干净? 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com