
题目列表(包括答案和解析)
下表是实验室制备气体的有关内容:
| 编号 | 实验内容 | 实验原理 | 气体发生装置 |
| ① | 制备氧气 | H2O2→O2 | |
| ② | 制备氨气 | NH4Cl→NH3 | |
| ③ | 制备氯气 | HCl→Cl2 |
(1) 从上述气体制备原理中:从制备过程看,必须选择合适的氧化剂才能实现
的是 (填气体的化学式,下同);从反应原理看,明显不同于其他两种气体的是 。
(2) 根据表中所列实验原理,从下列装置中选择合适的气体发生装置,将其编号填入上表中的空格中。

Ⅰ Ⅱ Ⅲ Ⅳ

(3) 某学习小组设计了如下图实验,将氯气依次通过下列装置以验证氯气的性质:
①通入氯气后,A中的现象是 ,整套实验装置存在的明显缺陷是 。
②C装置中发生反应的离子方程式为: 。
某课外活动小组加热炭粉(过量)和氧化铜的混合物,再用下图装置,对获得的铜粉(含炭)样品进行实验。图中铁架台等装置已略去。请你帮助他们完成下列实验报告。
(1)实验目的:________________________________________。
(2)实验用品:仪器:天平、分液漏斗、锥形瓶、硬质玻璃管、干燥管、酒精灯、洗气瓶等。药品:红褐色铜粉(含炭)样品、过氧化氢溶液、二氧化锰、碱石灰、浓硫酸等
(3)实验内容

实验步骤 实验现象 有关化学方程式
在G中加入样品粉末Wg,D中装入药品后并称量为m1g,连接好仪器后,检查气密性
打开A的活塞,慢慢滴加
溶液
对G进行加热。当G中药品充分反应后,关闭A的活塞,停止加热
冷却后,
称量D的质量为m2g
(4)计算:样品中铜的质量分数=________(用含W、m1、m2的代数式表示)
(5)问题和讨论:
实验完成后,老师评议说:“按上述实验设计,即使G中反应完全、D中吸收完全,也不会得出正确的结果。经讨论,有同学提出在B与G之间加入一个装置。再次实验后,得到了较正确的结果。那么,原来实验所测得的铜的质量分数偏小的原因可能是________。在B与G之间加入的装置可以是________________________。其中盛放的药品是____________
________________。
(1)实验目的:________________________________________。
(2)实验用品:仪器:天平、分液漏斗、锥形瓶、硬质玻璃管、干燥管、酒精灯、洗气瓶等。药品:红褐色铜粉(含炭)样品、过氧化氢溶液、二氧化锰、碱石灰、浓硫酸等
(3)实验内容
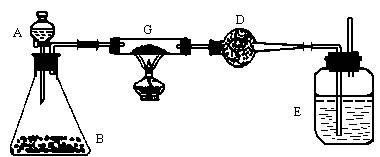
实验步骤 实验现象 有关化学方程式
在G中加入样品粉末Wg,D中装入药品后并称量为m1g,连接好仪器后,检查气密性
打开A的活塞,慢慢滴加
溶液
对G进行加热。当G中药品充分反应后,关闭A的活塞,停止加热
冷却后,
称量D的质量为m2g
(4)计算:样品中铜的质量分数=________(用含W、m1、m2的代数式表示)
(5)问题和讨论:
实验完成后,老师评议说:“按上述实验设计,即使G中反应完全、D中吸收完全,也不会得出正确的结果。经讨论,有同学提出在B与G之间加入一个装置。再次实验后,得到了较正确的结果。那么,原来实验所测得的铜的质量分数偏小的原因可能是________。在B与G之间加入的装置可以是________________________。其中盛放的药品是____________
________________。
(14分)某研究性学习小组在网上收集到如下信息:Fe(NO3)3溶液可以蚀刻银,制作美丽的银饰。他们对蚀刻银的原因进行了如下探究:
【实验】制作银镜,并与Fe(NO3)3溶液反应,发现银镜溶解。
(1)下列有关利用Fe粉与稀HNO3制备Fe(NO3)3溶液的方法,最佳的是 。
a.把过量的铁粉与稀HNO3反应
b.把铁粉与过量的稀HNO3反应
c.先把铁粉灼烧,再溶解于稀HNO3 中
【提出假设】
假设1:Fe3+具有氧化性,能氧化Ag。
假设2:Fe(NO3)3溶液显酸性,在此酸性条条件下NO3-能氧化Ag。
【设计实验方案,验证假设】
(2)甲同学为了验证假设1,取上述实验后的溶液,检验Fe2+。
检验Fe2+的方法: ,甲同学观察到的实验现象为: ,
甲同学检验出Fe2+,验证了假设1的成立。请写出Fe3+氧化Ag的离子方程式: 。
(3)乙同学设计实验验证假设2,请帮他完成下表中内容(提示:NO3-在不同条件下的还原产物较复杂,有时难以观察到气体产生,乙同学放弃了检验NO3-在不同条件下的还原产物的方法)。
| 实验步骤(不要求写具体操作过程) | 预期现象和结论 |
| ① | 若银镜消失,假设②成立。 若银镜不消失,假设②不成立。 |
| ② |
(16分)某研究性学习小组在网上收集到如下信息:Fe(NO3)3溶液可以蚀刻银,制作美丽的银饰。他们对蚀刻银的原因进行了如下探究:
【实验】制作银镜,并与Fe(NO3)3溶液反应,发现银镜溶解。
(1)下列有关利用Fe粉与稀HNO3制备Fe(NO3)3溶液的方法,最佳的是 。
a.把过量的铁粉与稀HNO3 反应
b.把铁粉与过量的稀HNO3 反应
c.先把铁粉灼烧,再溶解于稀HNO3 中
【提出假设】
假设1:Fe3+具有氧化性,能氧化Ag。
假设2:Fe(NO3)3溶液显酸性,在此酸性条件下NO3-能氧化Ag。
【设计实验方案,验证假设】
(2)甲同学为了验证假设1,取上述实验后的溶液,检验Fe2+。检验Fe2+的方法: ,甲同学观察到的实验现象为: ,甲同学检验出Fe2+,验证了假设1的成立。请写出Fe3+氧化Ag的离子方程式: 。
(3)乙同学设计实验验证假设2。请写出在酸性条件下NO3-氧化Ag的离子方程式: 。并帮乙同学完成下表中内容(提示:NO3-在不同条件下的还原产物较复杂,有时难以观察到气体产生,乙同学放弃了检验NO3-在不同条件下的还原产物的方法)。
|
实验步骤(不要求写具体操作过程) |
预期现象和结论 |
|
①测定上述实验用的Fe(NO3)3溶液的pH值 |
|
|
② |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com