ЈЁ2013?өВЦЭДЈДвЈ©ўсЈ®№ӨТөЙПУГөзҪвИЫИЪСх»ҜВБөД·Ҫ·ЁАҙЦЖИЎҪрКфВБЈ®ҙҝҫ»Сх»ҜВБөДИЫөгәЬёЯЈЁФј2045ЎжЈ©Ј¬ФЪКөјКЙъІъЦРЈ¬НЁ№эјУИлЦъИЫјБұщҫ§КҜЈЁNa
3AlF
6Ј©ФЪ1000ЎжЧуУТҫНҝЙТФөГөҪИЫИЪМеЈ®
Нј1КЗөзҪвІЫөДКҫТвНјЈ®
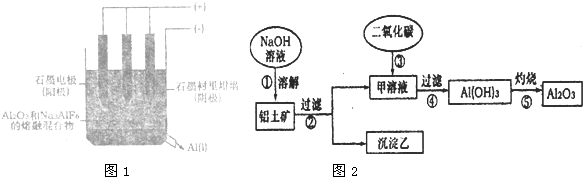
ЈЁ1Ј©РҙіцөзҪвКұТх°вөДөзј«·ҙУҰКҪ
Al3++3e-=Al
Al3++3e-=Al
Ј®
ЈЁ2Ј©өзҪв№эіМЦРЙъіЙөДСхЖшИ«ІҝУлКҜД«өзј«·ҙУҰЙъіЙC0әНC0
2ЖшМеЈ®ТтҙЛЈ¬РиТӘІ»¶ПІ№ідКҜД«өзј«Ј®№ӨТөЙъІъЦРЈ¬ГҝЙъІъ9tВБСфј«ЛрК§5.4tКҜД«Ј®ЙъіЙөД¶юСх»ҜМјөДОпЦКөДБҝОӘ
5ЎБ104
5ЎБ104
ўтЈ®№ӨТөЙПУГВБНБҝуЈЁЦчТӘіЙ·ЦКЗAl
2O
3Ј¬»№ә¬УРFe
20
3ЎўSi0
2Ј©МбИЎСх»ҜВБЧцТұБ¶ВБөДФӯБПЈ®ЖдЦРТ»ЦЦМбИЎөДЮъЧч№эіМИзЈЁНј2Ј©Јә
Зл»ШҙрПВБРОКМвЈә
ЈЁ1Ј©ЗлРҙіцјЧИЬТәЦРНЁИлЧгБҝ¶юСх»ҜМјЙъіЙЗвСх»ҜВБөДАлЧУ·ҪіМКҪ
AlO2-+CO2+2H2O=HCO3-+AlЈЁOHЈ©3Ўэ
AlO2-+CO2+2H2O=HCO3-+AlЈЁOHЈ©3Ўэ
Ј®
ЈЁ2Ј©іБөнТТКЗFe
20
3әНSi0
2өД»мәПОпЈ¬ПтЖдЦРјУИлЧгЦГСОЛбЈ¬Рҙіц·ҙУҰөДАлЧУ·ҪіМКҪ
Fe2O3+6H+ЁT2Fe3++3H2O
Fe2O3+6H+ЁT2Fe3++3H2O
Ј¬ід·Ц·ҙУҰәу№эВЛЈ¬Ҫ«ВЛТәјУИИХфёЙЧЖЙХЈ¬ЧоәуҝЙөГөҪәмәЦЙ«№ММеЈ¬УГјтТӘөДОДЧЦәН»ҜС§·ҪіМКҪЛөГчХвТ»ұд»Ҝ№эіМ
FeCl3+3H2O?FeЈЁOHЈ©3+3HClЈ¬јУИИҙЩҪшЛ®ҪвЈ¬ЗТСОЛбТЧ»У·ўЈ¬»ҜС§ЖҪәвХэПтТЖ¶ҜЈ¬ЙъіЙЗвСх»ҜМъЈ¬ЧоәуЧЖЙХЗвСх»ҜМъ·ЦҪвЙъіЙСх»ҜМъЈ¬2FeЈЁOHЈ©3ЁTFe2O3+3H2O
FeCl3+3H2O?FeЈЁOHЈ©3+3HClЈ¬јУИИҙЩҪшЛ®ҪвЈ¬ЗТСОЛбТЧ»У·ўЈ¬»ҜС§ЖҪәвХэПтТЖ¶ҜЈ¬ЙъіЙЗвСх»ҜМъЈ¬ЧоәуЧЖЙХЗвСх»ҜМъ·ЦҪвЙъіЙСх»ҜМъЈ¬2FeЈЁOHЈ©3ЁTFe2O3+3H2O
Ј®
ЈЁ3Ј©ЙПКцМбИЎСх»ҜВБөД·Ҫ·ЁҪРјоИЬ·ЁЈ®№ӨТөЙъІъЦР»№УРТ»ЦЦЛбИЬ·ЁЈ®
өЪТ»ІҪЈәПтВБНБҝуЦРјУСОЛбЈ¬И»әу№эВЛЈ»өЪ¶юІҪЈәҙҰАнөГөҪөДВЛТәЈ®ЗлДгЛјҝјөЪ¶юІҪІЩЧчЦРК№УГөД»ҜС§КФјБКЗ
NaOHИЬТә»тЗҝјоИЬТә
NaOHИЬТә»тЗҝјоИЬТә
Ј®

