
题目列表(包括答案和解析)
①金红石与炭粉混合高温放出可燃性气体 ②①中得到的固体与Cl2高温下反应得TiCl4 ③TiCl4经提纯后在Ar气中与过量Mg反应还原出Ti ④最后得到的Ti经酸水洗后得纯Ti
下列叙述错误的是( )
A.金属钛可作为航天器的材料
B.②的反应属于置换反应,Ar是保护气
C.酸洗的目的是除去钛中的镁
D.制备中放出的气体排入大气不会造成严重污染
金属钛的机械强度高、抗蚀能力强,被誉为“21世纪的金属”.工业上常用硫酸分解钛铁矿石( )的方法来制取二氧化钛,再由二氧化钛制取金属钛,主要反应有:
)的方法来制取二氧化钛,再由二氧化钛制取金属钛,主要反应有:
①
②
③
④
⑤
下列叙述中,错误的是
[ ]
A.反应①不是氧化还原反应
B.反应②是置换反应
C.反应④中 是氧化剂
是氧化剂
D.反应⑤表现了金属镁的还原性比金属钛的还原性强
金属钛的机械强度高、抗蚀能力强,被誉为“21世纪的金属”.工业上常用硫酸分解钛铁矿石(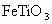 )的方法来制取二氧化钛,再由二氧化钛制取金属钛,主要反应有:
)的方法来制取二氧化钛,再由二氧化钛制取金属钛,主要反应有:
①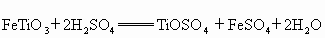
②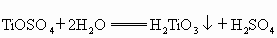
③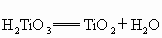
④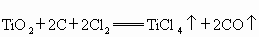
⑤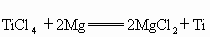
下列叙述中,错误的是
[ ]
A.反应①不是氧化还原反应
B.反应②是置换反应
C.反应④中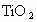 是氧化剂
是氧化剂
D.反应⑤表现了金属镁的还原性比金属钛的还原性强
金属钛(Ti)性能优越,被称为继铁、铝之后的“第三金属”。工业上以金红石为原料制取Ti的反应为:
aTiO2+bCl2+cC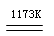 aTiCl4+cCO……反应①
aTiCl4+cCO……反应①
TiCl4+2Mg Ti+2MgCl2……反应②
Ti+2MgCl2……反应②
关于反应①②的分析不正确的是( )
A.TiCl4在反应①中是还原产物,在反应②中是氧化剂
B.C、Mg在反应中均为还原剂,被氧化
C.每生成0.4 mol Ti,反应①②中共转移3.2 mol e-
D.反应①②都是置换反应
| ||
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com