钠和氯是我们熟悉的典型金属元素与非金属元素,研究它们的性质对于生产、生活、科研具有重要意义.请回答以下问题:
(1)金属钠在空气中燃烧的产物,常用于呼吸面具中的供氧剂,其工作原理是(用化学反应方程式回答)
2Na2O2+2CO2=2Na2CO3+O2,2Na2O2+2H2O=4NaOH+O2↑
2Na2O2+2CO2=2Na2CO3+O2,2Na2O2+2H2O=4NaOH+O2↑
.
(2)某化学兴趣小组设计以下装置来验证Cl
2的性质.
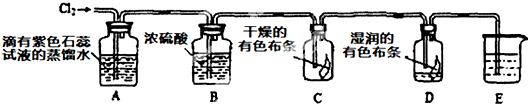
①装置A中的现象是
溶液先变红后褪色
溶液先变红后褪色
,发生反应的离子方程式为
Cl2+H2O=H++Cl-+HClO
Cl2+H2O=H++Cl-+HClO
,上述反应中若有336mL(标准状况)Cl
2参加反应,参加反应的还原剂的物质的量为
0.0075mol
0.0075mol
.
②装置B的作用是
干燥氯气
干燥氯气
.
③装置C与装置D中的现象是否相同
否
否
(填“是”或“否”),根据装置C和D中的现象可以得到的结论是
干燥的氯气没有漂白性
干燥的氯气没有漂白性
.
④装置E的作用是吸收尾气,盛放的试剂最好是
氢氧化钠溶液
氢氧化钠溶液
.

