
题目列表(包括答案和解析)
已知下列热化学方程式:Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g);△H="-24.8" kJ/mol
2Fe(s)+3CO2(g);△H="-24.8" kJ/mol
Fe2O3(s)+ 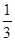 CO(g)
CO(g)
 Fe3O4(s)+
Fe3O4(s)+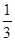 CO2(g);△H="-15.73" kJ/mol
CO2(g);△H="-15.73" kJ/mol
Fe3O4(s)+ CO(g) 3FeO(s)+CO2(g);△H="+640.4" kJ/mol
3FeO(s)+CO2(g);△H="+640.4" kJ/mol
则14 g CO气体还原足量FeO固体得到Fe固体和CO2气体时对应的ΔH约为 ( )
| A.-218 kJ/mol | B.-109 kJ/mol | C.+218 kJ/mol | D.+109 kJ/mol |
已知下列热化学方程式:
(1)Fe2O3(s)+3CO(g)![]() 2Fe(s)+3CO2(g);ΔH=-25 kJ/mol
2Fe(s)+3CO2(g);ΔH=-25 kJ/mol
(2)3Fe2O3(s)+CO(g)![]() 2Fe3O4(s)+CO2(g);ΔH=-47 kJ/mol
2Fe3O4(s)+CO2(g);ΔH=-47 kJ/mol
(3)Fe3O4(s)+CO(g)![]() 3FeO(s)+CO2(g);ΔH=+19 kJ/mol
3FeO(s)+CO2(g);ΔH=+19 kJ/mol
写出FeO(s)被CO还原成Fe和CO2的热化学方程式________.
(3分)已知下列热化学方程式
Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g);ΔH=-25kJ/mol
3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g);ΔH=-47kJ/mol
3Fe3O4(s)+CO(g)=3FeO(s)+CO2(g);ΔH=+19kJ/mol
写出FeO(s)被CO(g)还原成Fe(s)和CO2(g)的热化学方程式:
已知;①Fe(s)+CO2(g)
 FeO(s)+CO(g) ΔH=a kJ·mol-1,平衡常数为K;
FeO(s)+CO(g) ΔH=a kJ·mol-1,平衡常数为K;
②Fe2O3(s)+3CO(g)===2Fe(s)+3CO2(g) ΔH=b kJ·mol-1。
测得在不同温度下,K值如下:
| 温度/℃ | 500 | 700 | 900 |
| K | 1.00 | 1.47 | 2.40 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com