
题目列表(包括答案和解析)
 验室用需配制250mL 0.1mol/L的Na2CO3溶液,填空并请回答下列问题:
验室用需配制250mL 0.1mol/L的Na2CO3溶液,填空并请回答下列问题:| 实际应称Na2CO3质量/g | 应选用容量瓶的规格/mL | 除容量瓶外还需要的其它仪器 |
| 2.7g | 250ml | 玻璃棒、烧杯、胶头滴管 |
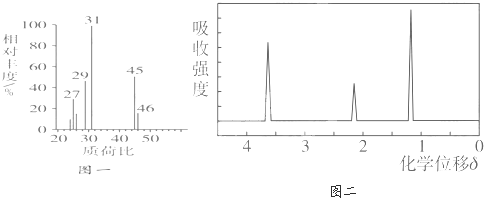
| 分子式 | 相对分子质量 | 溶解度和溶解性 | 酸性 |
| H4C4O4 | 116 | 在水中:0.7g(25℃)、9.8g(97.5℃). 盐酸中:可溶. |
二元酸,且0.1mol/L H4C4O4的pH=2. |
| 开始沉淀时的pH | 完全沉淀时的pH |
| 7.6 | 9.6 |
富马酸亚铁FeH2C4O4,商品名富血铁,含铁量高,是治疗缺铁性贫血常见的药物。某校研究性学习小组通过查阅大量资料后,决定自行制备富血铁并检测其含铁量。
富马酸(HOOC-CH=CH-COOH)的性质:
| 分子式 | 相对分子质量 | 溶解度和溶解性 | 酸性 |
| H4C4O4 | 116 | 在水中:0.7g(25℃)、9.8g (97.5℃)。 盐酸中:可溶。 | 二元酸,且0.1mol/LH4C4O4的pH=2。 |
Fe2+的性质:
| 开始沉淀时的pH | 完全沉淀时的pH |
| 7.6 | 9.6 |
I、富马酸亚铁的制备
①将适量的富马酸置于100ml烧杯中,加水20ml在热沸搅拌下,加入Na2CO3溶液10ml,使其pH为6.5~6.7;
②将上述溶液转移至100ml圆底烧瓶中,装好回流装置,加热至沸;
③缓慢加入新制的FeSO4溶液30ml,维持温度100℃,充分搅拌1.5小时。
④冷却、过滤,洗涤沉淀,然后水浴干燥,得到棕色粉末。
试回答:
步骤①中加入Na2CO3 ,反应的离子方程式_____________(富马酸及其酸根用化学式表示)。
步骤①中反应后控制溶液pH为6.5~6.7;若反应后溶液的pH太小,则引起的后果是_____________。若反应后溶液的pH太大则引起的后果是__________________。
II 产品纯度测定
准确称取富血铁0.3200g,加煮沸过的3mol/LH2SO4溶液15ml,待样品完全溶解后,加煮沸过的冷水50ml和4滴邻二氮菲-亚铁指示剂,立即用(NH4)2Ce(SO4)3(硫酸高铈铵)0.1000mol/L标准溶液进行滴定。直至溶液刚好变为浅蓝色即为终点。测得其体积为18.50mL,计算样品中富血铁的质量分数,写出计算过程。(Fe2+ +Ce4+=Fe3+ + Ce3+)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com