
题目列表(包括答案和解析)
| 滴定次数 实验数据 |
1 | 2 | 3 | 4 |
| V(样品)/mL | 20.00 | 20.00 | 20.00 | 20.00 |
| V(NaOH)/mL(初读数) | 0.00 | 0.200 | 0.10 | 0.00 |
| V(NaOH)/mL(终读数) | 14.98 | 15.20 | 15.12 | 15.95 |
| V(NaOH)/mL(消耗) | 14.98 | 15.00 | 15.02 | 15.95 |
| V(NaOH)/mL | 0.00 | 10.00 | 18.00 | 19.80 | 19.98 | 20.00 | 20.02 | 20.20 | 22.00 |
| 溶液pH | 2.88 | 4.70 | 5.70 | 6.74 | 7.74 | 8.72 | 9.70 | 10.70 | 11.70 |
| 指示剂 | 变色的范围(pH) |
| 甲基橙 | 3.1~4.4 |
| 石蕊 | 5.0~8.0 |
| 酚酞 | 8.2~10.0 |
某烧碱溶液中含有少量杂质(不与盐酸反应),现用中和滴定测定其浓度.
(1)滴定
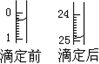
①用酸式滴定管盛装c mol/L盐酸标准液.下图表示某次滴定时50 mL滴定管中滴定前后液面的位置.用去的标准盐酸的体积为________mL.
②下表是4种常见指示剂的变色范围:
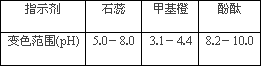
该实验应选用________作指示剂;
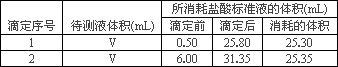
③有关数据记录如下:
(2)根据1、2所给数据,写出计算烧碱样品的物质的量浓度的表达式(不必化简)
c=________.
(3)对下列几种假定情况进行讨论:(填“无影响”、“偏高”、“偏低”)
a.若滴定前用蒸馏水冲洗锥形瓶,则会使测定结果________;
b.读数时,若滴定前仰视,滴定后俯视,则会使测定结果________;
c.滴加盐酸速度过快,未充分振荡,刚看到溶液变色,立刻停止滴定,则会使测定结果________.
某实验小组拟用酸碱中和滴定法测定食醋的总酸量(g/100 mL),现邀请你参与本实验并回答相关问题.(有关实验药品为:市售食用白醋样品500 mL、0.1000 mol/LNaOH标准溶液、蒸馏水、0.1%甲基橙溶液、0.1%酚酞溶液、0.1%石蕊溶液.)
Ⅰ.实验步骤:
(1)用滴定管吸取10 mL市售白醋样品,置于100 mL容量瓶中,加蒸馏水(煮沸除去CO2并迅速冷却))稀释至刻度线,摇匀即得待测食醋溶液.
(2)用酸式滴定管取待测食醋溶液20.00 mL于________中.
(3)盛装标准NaOH溶液,静置后,读取数据,记录为NaOH标准溶液体积的初读数.
(4)滴定,并记录NaOH的终读数.重复滴定2-3次.
Ⅱ.实验记录及数据处理
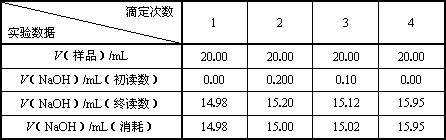
则c(样品)/moL·L-1=________;样品总酸量g / 100mL=________.
Ⅲ.交流与讨论:
(1)甲同学在处理数据过程中计算得:
V(NaOH)(平均消耗)=1/4(14.98+15.00+15.02+15.95)mL=15.24 mL.
试分析他的计算是否合理,如果不合理请说明理由.
________________________________________________________________.
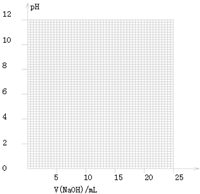
(2)乙同学用0.1000 mol/L NaOH溶液滴定另一市售白醋样品溶液时,滴定过程中使用pH计将溶液的pH变化情况记录如下表.
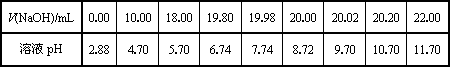
①请作出pH-V(NaOH)图.
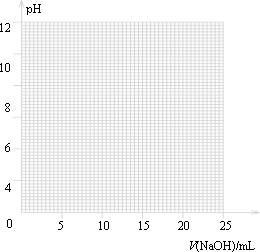
①由表和图可知:在允许的误差范围(±0.1%)内,pH突变
(滴定突跃)范围为________.
所以可选择________作指示剂.
附:常见指示剂的变色范围

某烧碱溶液中含有少量杂质(不与盐酸反应),现用中和滴定测定其浓度.
(1)滴定
①用________式滴定管盛装c mol/L盐酸标准液.下图表示某次滴定时50 mL滴定管中前后液面的位置.请将用去的标准盐酸的体积填入③表空格中,此时滴定管中液体的体积为________mL.

②下表是4种常见指示剂的变色范围:
该实验应选用________作指示剂;
③有关数据记录如下:

(2)根据所给数据,写出计算烧碱样品的物质的量浓度的表达式(不必化简)
c=________.
(3)对下列几种假定情况进行讨论:(填“无影响”、“偏高”、“偏低”)
a.若滴定前用蒸馏水冲洗锥形瓶,则会使测定结果________;
b.读数时,若滴定前仰视,滴定后俯视,则会使测定结果________;
c.若在滴定过程中不慎将数滴酸液滴在锥形瓶外,则会使测定结________;
d.滴加盐酸速度过快,未充分振荡,刚看到溶液变色,立刻停止滴定,则会使测定结果________.
某烧碱溶液中含有少量杂质(不与盐酸反应),现用中和滴定测定其浓度。
(1)滴定:①用 式滴定管盛装c mol/L盐酸标准液。如图表示某次滴定时50 mL滴定管中前后液面的位置。请将用去的标准盐酸的体积填入③表空格中,此时滴定管中液体的体积 mL。
②下表是4种常见指示剂的变色范围: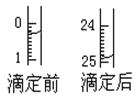
| 指示剂 | 石蕊 | 甲基橙 | 甲基红 | 酚酞 |
| 变色范围(pH) | 5.0—8.0 | 3.1—4.4 | 4.4—6.2 | 8.2—10.0 |
| 滴定序号 | 待测液体积(mL) | 所消耗盐酸标准液的体积(mL) | ||
| 滴定前 | 滴定后 | 消耗的体积 | ||
| 1 | V | 0.50 | 25.80 | 25.30 |
| 2 | V | | | |
| 3 | V | 6.00 | 31.35 | 25.35 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com