
题目列表(包括答案和解析)
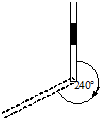
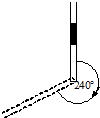 如图所示,一端开口一端封闭的粗细均匀的直玻璃管,长为1m,开口向上竖直放置时,一段长为15cm的水银柱封闭了一段长50cm的气柱,若保持温度不变,将玻璃管在竖直平面内缓慢地顺时针旋转240°角,则最终管内气柱长为多少?已知大气压强为p0=75cmHg.某同学对此题的分析为:封闭气体的初始状态的空气柱长为50cm,压强为(75+15)cmHg;末状态的压强为(75-
如图所示,一端开口一端封闭的粗细均匀的直玻璃管,长为1m,开口向上竖直放置时,一段长为15cm的水银柱封闭了一段长50cm的气柱,若保持温度不变,将玻璃管在竖直平面内缓慢地顺时针旋转240°角,则最终管内气柱长为多少?已知大气压强为p0=75cmHg.某同学对此题的分析为:封闭气体的初始状态的空气柱长为50cm,压强为(75+15)cmHg;末状态的压强为(75-| 15 | 2 |
| 15 |
| 2 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com