
题目列表(包括答案和解析)
请你与某小组的同学共同进行乙醇与乙酸酯化反应的探究实验:
⑴要向大试管中加2mL浓硫酸、3mL乙醇、2mL乙酸,其具体操作是: 。
⑵下边是实验室制取乙酸乙酯的装置图,其中小试管中装入的物质是 。

⑶分离小试管中制取的乙酸乙酯应使用的仪器叫做 ;分离时,乙酸乙酯应该从仪器
(填:“下口放” 或“上口倒”) 出。
⑷实验完毕,发现大试管中的反应液有些变黑,其原因是 。
⑸他们反复实验,得出乙醇与乙酸用量和最后得到的乙酸乙酯生成量如下表:
| 实验 | 乙醇(mL) | 乙酸(mL) | 乙酸乙酯(mL) |
| ① | 2 | 2 | 1.33 |
| ② | 3 | 2 | 1.57 |
| ③ | 4 | 2 | X |
| ④ | 5 | 2 | 1.76 |
| ⑤ | 2 | 3 | 1.55 |
表中数据X的范围是 ;实验①与实验⑤探究的目的是 ;
若乙醇价格为500元/kmol,乙酸价格为800元/kmol,乙酸乙酯价格为1600元/kmol,结合表中实验②③④的数据,你能得出的结论是 。
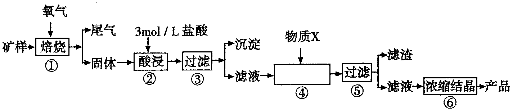
| 金属离子 | 开始形成氢氧化物沉淀的pH | 完全形成氢氧化物沉淀的pH |
| Fe2+ | 7.0 | 9.0 |
| Fe3+ | 1.9 | 3.2 |
| Cu2+ | 4.7 | 6.7 |
| ||
| ||
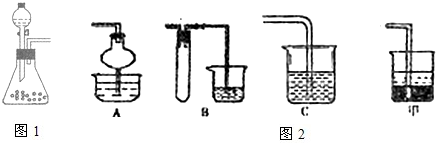
某化学兴趣小组的同学们探究乙醇与乙酸的酯化反应实验________________________。
(1) 要向大试管中加2 mL 浓硫酸、3 mL乙醇、2mL乙酸,其具体操作是:________________________________________________________。
(2)请根据图示,补画实验室制取乙酸乙酯的装置图。其中小试管中装入的物质是_______。

(3)分离小试管中制取的乙酸乙醋应使用的仪器叫做______________;分离完毕,应从该仪器______________(填“下口放”或“上口倒”)出。
(4)实验中加热试管的目的除了加快反应速率外,依据平衡移动原理,还有___________________。
⑸实验完毕,发现大试管中的反应液有些变黑,其原因是____________________________。
(6)他们反复实验,得出乙醇与乙酸的用量和最后得到的乙酸乙酯生成量如下表:
| 编号 | 乙醇(mL) | 乙酸(mL) | 乙酸乙酯(mL) |
| 1 | 2 | 2 | 1.33 |
| 2 | 3 | 2 | 1.57 |
| 3 | 2 | 3 | 1.55 |
结合表中数据,你能得出的结论是____________________________________________。
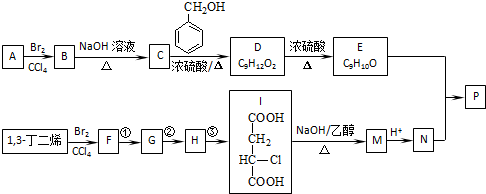
| KMnO3/H+ |
| 浓硫酸 |
| △ |
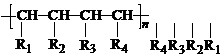 nCH=CH+nCH=CH
nCH=CH+nCH=CH| 催化剂 |



湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com