
题目列表(包括答案和解析)
下列各离子组的叙述正确的是 ( )
A.在强酸性条件下Na+、IO-、K+、可以大量共存
B.在强碱性条件下K+、AlO2-、Na+、NO3—可以大量共存
C.在水溶液中H+、NH4+、SiO32—、Cl-不能大量共存
D.在强酸性条件下NH4+、K+、SO32—、S2-可以大量共存
下列各离子组的叙述正确的是 ( )
A.在强酸性条件下Na+、IO-、K+、可以大量共存
B.在强碱性条件下K+、AlO2-、Na+、NO3—可以大量共存
C.在水溶液中H+、NH4+、SiO32—、Cl-不能大量共存
D.在强酸性条件下NH4+、K+、SO32—、S2-可以大量共存
下列各离子组的叙述正确的是 ( )
A.在强酸性条件下Na+、IO-、K+、可以大量共存
B.在强碱性条件下K+、AlO2-、Na+、NO3—可以大量共存
C.在水溶液中H+、NH4+、SiO32—、Cl-不能大量共存
D.在强酸性条件下NH4+、K+、SO32—、S2-可以大量共存
下列各离子组的叙述正确的是 ( )
| A.在强酸性条件下Na+、IO-、K+、可以大量共存 |
| B.在强碱性条件下K+、AlO2-、Na+、NO3—可以大量共存 |
| C.在水溶液中H+、NH4+、SiO32—、Cl-不能大量共存 |
| D.在强酸性条件下NH4+、K+、SO32—、S2-可以大量共存 |
(16分)(1)(6分)测定Na2O和Na的混合物中金属钠的质量分数可用下图所示的几套仪器组合: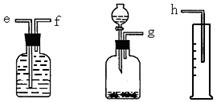
①用接口字母标出各仪器连接的顺序 量筒在实验中的作用是
②有一块表面氧化成Na2O的金属钠,其质量为2.0g,实验后在量筒中收集到0.224L水,求样品中金属钠的质量分数是 。(假设在标准状况下测定)
(2)(10分) HNO2是一种弱酸,且不稳定,易分解生成NO和NO2;它能被常见的强氧化剂氧化;在酸性溶液中它也是一种氧化剂,如能把Fe2+氧化成Fe3+。AgNO2是一种难溶于水、易溶于酸的化合物。试回答下列问题:
①人体正常的血红蛋白含有Fe2+。若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转化为Fe3+而中毒,服用维生素C可解毒。下列叙述不正确的是________(填序号)。
A.亚硝酸盐被还原 B.维生素C具有还原性
C.维生素C将Fe3+还原为Fe2+ D.在上述变化中亚硝酸盐是还原剂
②下列方法中,不能用来区分NaNO2和NaCl两种溶液的是________(填序号)。
A.测定这两种溶液的pH
B.分别在两种溶液中滴加甲基橙
C.在酸性条件下加入KI—淀粉溶液来区别
D.用AgNO3和HNO3两种试剂来区别
③某同学把新制的氯水加到NaNO2溶液中,观察到氯水褪色,同时生成NaNO3和HCl,请写出反应的离子方程式:___________________________________。
④ Fe与过量稀硫酸反应可以制取FeSO4。若用反应所得的酸性溶液,将Fe2+转化为Fe3+,要求产物纯净,可选用的最佳试剂是________(填序号)。
a.Cl2 b.Fe c.H2O2 d.HNO3
⑤配平下列方程式:
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com