
题目列表(包括答案和解析)
 人们对苯的结构及性质的认识经历了一个漫长的过程.
人们对苯的结构及性质的认识经历了一个漫长的过程. +Br
+Br| 催化剂 |
 -Br+HBr
-Br+HBr +Br
+Br| 催化剂 |
 -Br+HBr
-Br+HBr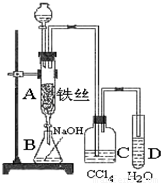
(14分)已知硝酸锏溶液颜色为蓝色.某学校化学课外小组同学们在做铜与浓硝酸、稀硝酸反应的实验中,发现铜和浓硝酸反应后溶液为绿色旦有红棕色气体产生,而铜和稀硝酸反应后溶液为蓝色,产生无色气体.为弄清反应后溶液颜色出现差异的原因,他们进行了实验探究.
[实验]在两支试管中各放入一小块等质量的铜片,分别加人等体积的浓HN03(14 mol •
L-1)和稀HN03(4mol . L-1 ), 立即用蘸有NaOH的棉花封住试管口。充分反应后铜均无剩余。
(1) Cu与浓HNO3反应的离子方程式________________________________
(2) 用蘸有NaOH的棉花封住试管口的原因________________
已知NO2与NaOH溶液反应中,其中NO2的还原产物是亚硝酸盐(NO2- )
写出反应的化学反应式________________________,
[提出假设]假设一、因为铜离子浓度大造成的。
假设二、溶液呈绿色是因为铜与浓硝酸反应时产生的二氧化氮溶于过量浓硝酸,加上和蓝色的硝酸铜溶液混在一起,使溶液呈绿色。
[设计实验方案,验证假设]
(3) 上述实验________(“能”或“不能”)证明假设一不成立,原因________________
(4) 甲同学设计实验验证假设二,请帮他完成下表中内容(提示:NO3-在不同条件下的还咬产物较复杂,有时难以观察到气体产生)

[分析推理】
(5)铜和稀硝酸反应后溶液为蓝色的原理________________
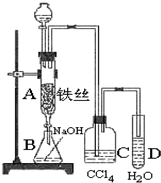
(14分)某中学课外兴趣小组用惰性电极电解饱和食盐水(含少量Ca2+、Mg2+)作系列探究,装置如下图所示:
(1)电解时,甲同学发现电极a附近溶液出现浑浊,请用离子方程式表示原因____________
(2)一段时间后,你认为C中溶液可能出现的现象是______,请用离子方程式表示原因________________________
(3) 实验结束后,乙同学将A中的物质冷却后加入到H2S溶液中发现有气泡出现,但加人到稀盐酸中却没有任何现象。请用化学方程式和简要的文字解释原因____________
(4) 随着反应的进行,兴趣小组的同学们都特别注意到D中溶液红色逐渐褪去。他们对溶液红色褪去主要原因提出了如下假设,请你完成假设二。
假设一:B中逸出气体与水反应生成的物质有强氧化性,使红色逐渐褪去;
假设二 :__________________________________________。
(5) 请你设计实验验证上述假设一,写出实验步骤及结论___________________________________________________________________________
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com