
题目列表(包括答案和解析)
(12分)A、B、C、D、E是除稀有气体以外的的5种短周期元素,原子序数依次增大并分占三个周期。B、C、D为同一周期依次相邻的3种元素,B和D的原子序数之比为3 :4,E原子的电子层数等于最外层电子数。请回答相关问题:
(1)B元素在周期表中的位置_______________,C元素是__________(填元素符号)
(2)比较D和E简单离子半径的大小(用离子符号表示):__________________
(3)A和D形成的含18电子化合物的化学式为___________________
(4)元素E形成的简单离子的水溶液与C的氢化物的水溶液反应的离子方程式为: ________________________________________________
(5)2007年7月2日,美、德两国科学家成功合成了具有独特化学特性的E2A6化合物,该物质在D2中能燃烧,写出它在D2中完全燃烧的化学方程式: _________________________________________
(12分)A、B、C、D、E是除稀有气体以外的的5种短周期元素,原子序数依次增大并分占三个周期。B、C、D为同一周期依次相邻的3种元素,B和D的原子序数之比为3 :4,E原子的电子层数等于最外层电子数。请回答相关问题:
(1)B元素在周期表中的位置_______________,C元素是__________(填元素符号)
(2)比较D和E简单离子半径的大小(用离子符号表示):__________________
(3)A和D形成的含18电子化合物的化学式为___________________
(4)元素E形成的简单离子的水溶液与C的氢化物的水溶液反应的离子方程式为:________________________________________________
(5)2007年7月2日,美、德两国科学家成功合成了具有独特化学特性的E2A6化合物,该物质在D2中能燃烧,写出它在D2中完全燃烧的化学方程式: _________________________________________
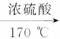
请回答下列问题:
(1)简述乙烯的一种重要工业用途:_____________________。
(2)实验室制取乙烯的化学方程式为________________________。
(3)D的结构简式为__________________。
(4)I(C6H10O4)有多种同分异构体,其中符合HOOC—COOC4H9的同分异构体共有___________种。
(5)写出下列转化的化学方程式并指出指定反应的反应类型。
E![]() F:__________________________。
F:__________________________。
G+H![]() I:___________________,反应类型:_________________________。
I:___________________,反应类型:_________________________。

请回答下列问题:
(1)简述乙烯的一种重要工业用途:___________________________________________。
(2)实验室制取乙烯的化学方程式为__________________________________。
(3)D的结构简式为__________________________________。
(4)I(C6H10O4)有多种同分异构体,其中符合HOOC—COOC4H9的同分异构体共有______________种。
(5)写出下列转化的化学方程式并指出指定反应的反应类型。
E![]() F:__________________________________。
F:__________________________________。
G+H![]() I:___________________________,反应类型:_________________。
I:___________________________,反应类型:_________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com