
题目列表(包括答案和解析)
| ||
| ||
| A.1molH2的能量高于2molH具有的总能量 |
| B.反应物所具有的总能量高于生成物所具有的总能量 |
| C.断开1molH-H键和断开1molCl-Cl键所吸收的总能量小于形成2molH-Cl键所放出的总能量 |
| D.该反应中,化学能部分转变为热能 |
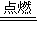 2HCl,下列说法不正确的是( )
2HCl,下列说法不正确的是( ) 对于放热反应H2 + Cl2 ![]() 2HCl,下列说法正确的是:
2HCl,下列说法正确的是:
A.1molH2所具有的总能量高于2molHCl所具有的总能量.
B.反应物所具有的总能量高于产物所具有的总能量
C.断开1mol H—H键和1mol Cl—Cl键所吸收的总能量大于形成2mol H—Cl键所放出的能量
D.该反应中,只有化学能转变为热能
[ ]
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com