
题目列表(包括答案和解析)
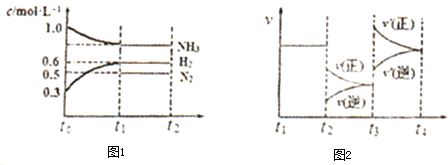
| A、若容器内气体的密度不再发生变化,则说明反应达到平衡状态 | B、若t1=20s,则从to-t1内的平均反应速率v(NH3)=0.01 mol?L-1 | C、图2中,t2时改变的条件是降低温度,t3时改变的条件是增大压强 | D、若t2时,再向容器中加入1.4 mol NH3、0.8 mol H2,则平衡将逆向移动 |
某化学反应2AB+D在三种不同条件下进行,B、D的起始浓度为0,反应物A的浓度(mol·L-1)随反应时间(min)的变化情况如下表:
根据表中数据,完成下列填空:
(1)在实验1中,A在10~20 min内的平均速率为 ;
(2)在实验2中,A的初始浓度c2为 mol·L-1,反应经20 min就达到平衡,可推测实验2中隐含的条件是 。
(1)已知25℃时有关弱酸的电离平衡常数:
|
弱酸化学式 |
HSCN |
CH3COOH |
HCN |
H2CO3 |
|
电离平衡常数 |
1.3×10—1 |
1.8×10—5 |
4.9×10—10 |
K1=4.3×10—7 K2=5.6×10—11 |
①等物质的量浓度的a.CH3COONa、b.NaCN、c.Na2CO3、d.NaHCO3溶液的pH由大到小的顺序为
(填序号)。
②25℃时,将20 mL 0.1 mol·L—1 CH3COOH溶液和20 mL 0.1 mol·L—1HSCN溶液分别与20 mL 0.1 mol·L—1NaHCO3溶液混合,实验测得产生的气体体积(V)随时间(t)的变化如图所示:反应初始阶段两种溶液产生CO2气体的速率存在明显差异的原因是 。反应结束后所得两溶液中,c(CH3COO—) c(SCN—)(填“>”、“<”或“=”)

③若保持温度不变,在醋酸溶液中加入少量盐酸,下列量会变小的是______(填序号)。
a. c(CH3COO-) b. c(H+) c. Kw d. 醋酸电离平衡常数
(2)下图为某温度下,PbS(s)、ZnS(s)、FeS(s)分别在溶液中达到沉淀溶解平衡后,溶液的S2—浓度、金属阳离子浓度变化情况。如果向三种沉淀中加盐酸,最先溶解的是 (填化学式)。向新生成的ZnS浊液中滴入足量含相同浓度的Pb2+、Fe2+的溶液,振荡后,ZnS沉淀会转化为 (填化学式)沉淀。

(3)甲烷燃料电池可以提升能量利用率。下图是利用甲烷燃料电池电解50 mL 2 mol·L—1的氯化铜溶液的装置示意图:

请回答:
① 甲烷燃料电池的负极反应式是 。
② 当线路中有0.1 mol电子通过时, 极增重________g
某化学反应2A B+D在三种不同条件下进行,B、D的起始浓度为0,反应物A的浓度(mol·L-1)随反应时间(min)的变化情况如下表:
B+D在三种不同条件下进行,B、D的起始浓度为0,反应物A的浓度(mol·L-1)随反应时间(min)的变化情况如下表:

根据表中数据,完成下列填空:
(1)在实验1中,A在10~20 min内的平均速率为 ;
(2)在实验2中,A的初始浓度c2为 mol·L-1,反应经20 min就达到平衡,可推测实验2中隐含的条件是 。
某研究性学习小组,对化学反应2A(g)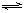 B(g)+D(g)在三种不同条件下进行实验,B、D起始浓度都为0,反应物A的浓度(mol/L) 随反应时间(min)的变化情况的实验数据如下表:
B(g)+D(g)在三种不同条件下进行实验,B、D起始浓度都为0,反应物A的浓度(mol/L) 随反应时间(min)的变化情况的实验数据如下表:
根据上述数据,回答下列问题:
(1)实验1中,10~20min时间内A的平均反应速率为__________mol/(L?min)。
(2)实验2中,隐含的反应条件可能是__________。
(3)实验3中,A的起始浓度____(填“>”、“<”或“=”,下同)1.0mol/L,起始反应速率_________实验1。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com