(2009?梅州模拟)柴达木盆地以青藏高原“聚宝盆”之誉蜚声海内外,它有富足得令人惊讶的盐矿资源.液体矿床以钾矿为主,伴生着镁、溴等多种矿产.某研究性学习小组拟取盐湖苦卤的浓缩液(富含K
+、Mg
2+、Br
-、SO
42-、Cl
-等),来制取较纯净的氯化钾晶体及液溴(Br
2),他们设计了如下流程图1:

请根据以上流程,回答相关问题:
(1)操作①的名称:
萃取
萃取
;操作②名称是:
分液
分液
;
操作③的名称是:
蒸馏
蒸馏
;
操作④需要的玻璃仪器有:
玻璃棒、漏斗、烧杯
玻璃棒、漏斗、烧杯
.
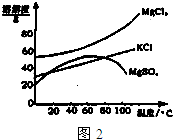
(2)参照图2溶解度曲线,欲得到较纯的氯化钾晶体需用少量的
冷水
冷水
(选填:“热水”,“冷水”)洗涤固体
B
B
(选填“A”或“B”).
(3)同学甲提出一些新的方案,对上述操作②后无色溶液进行除杂提纯,其方案如下:
【有关资料】
| 化学式 |
BaCO3 |
BaSO4 |
Ca(OH)2 |
MgCO3 |
Mg(OH)2 |
| Ksp |
8.1×10一9 |
1.08×10一10 |
1.0×10一4 |
3.5×10一5 |
1.6×10一11 |
【设计除杂过程】

(i)若在图3的操作⑤结束后发现溶液B略有浑浊,应采取的措施是
更换滤纸,重新过滤
更换滤纸,重新过滤
,
(ii)混合液A的主要成分是
BaCl2和KOH
BaCl2和KOH
.(填化学式)
【检验除杂效果】
(ⅲ)为检验Mg
2+、SO
42-是否除尽,通常分别取悬浊液A上层清液于两试管中.进行如下实验:
步骤一:检验Mg
2+是否除尽.向其中一支试管中加入
KOH
KOH
溶液(填化学式),如果没有沉淀生成,则Mg
2+已除尽.
步骤二:检验SO
42-是否除尽.向另一支试管中加入某溶液,如果无有沉淀生成,则SO
42-已除尽,效果最好的是
B
B
(填字母).
A.Na
2 CO
3 B.BaCl
2 C.CaCl
2【获取纯净氯化钾】
(ⅳ)对溶液B加热并不断滴加l mol?L
一1的盐酸溶液,同时用pH试纸检测溶液,直至pH=5时停止加盐酸,得到溶液C.该操作的目的是
加盐酸调节至pH=5目的是除去未反应的OH-和CO32-
加盐酸调节至pH=5目的是除去未反应的OH-和CO32-
.
(ⅴ)将溶液C倒入
蒸发皿
蒸发皿
(填仪器名称)中,加热蒸发并用玻璃棒不断搅拌,直到
出现较多晶体,剩余较少水时
出现较多晶体,剩余较少水时
时(填现象),停止加热.
【问题讨论】
(ⅵ)进行操作⑤前,需先加热,其目的是
使沉淀颗粒增大,便于过滤
使沉淀颗粒增大,便于过滤
,该操作中控制溶液pH=12可确保Mg
2+除尽,根据提供的数据计算,此时溶解B中Mg
2+物质的量浓度为
1.6×10一7mol/L
1.6×10一7mol/L
.




