
题目列表(包括答案和解析)

【化学——物质结构与性质】
氮及其化合物在生活生产和科技等方面有重要的应用。请回答下列问题:
(1)氮元素基态原子的价电子排布式为 ;
(2)在氮气分子中,氮原子之间存在着 个σ键和 个π键;
(3)磷、氨、氧是周期表中相邻的三种元素,比较:
①氮原子的第一电离能 (填“大于”、“小于”或“等于”)氧原子的第一电离能;
②N2分子中氮氮键的键长 (填“大于”、“小于”或“等于”)白磷分子中磷磷键的键长;
(4)氮元素的氢化物——NH3是一种易液化的气体,氨分子中氮原子杂化类型为 杂化,该气体易液化的原因是 。
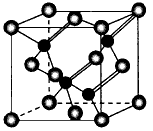
 【化学--选修3:物质结构与性质】
【化学--选修3:物质结构与性质】
| ||
| 2 |
| ||
| 2 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com