
题目列表(包括答案和解析)
| 实验内容 | 实验现象 | 结论 |
| ①分别取等体积的2mol/L硫酸于试管中; ②分别投入大小、形状相同的Cu、Fe、Mg. |
反应快慢: Mg |
反应物的性质越 |
影响化学反应速率的因素
内因:________.
外因
①浓度
在其他条件不变的情况下,增大反应物浓度,可以________化学反应速率;减小反应物浓度,可以________化学反应速率.
②温度
当其他条件不变时,升高温度可以________化学反应速率;降低温度可以________化学反应速率.
③反应物间的接触面积
其他条件不变时,反应物间的接触面积越大,化学反应速率________.
④催化剂
多数情况下,使用催化剂能够________化学反应速率.
⑤压强
对于有气体参加的化学反应,当其他条件不变时,增大压强可以________化学反应速率;减小压强可以________化学反应速率.
⑥光波、电磁波、超声波、溶剂等也会对化学反应速率产生影响.
(15分)广义的化学反应速率可以用参加化学反应的任一种物质“在单位时间内某一可测的物理量的变化量”来表示,即V(A) = ![]() ,rX(A)表示物质A物理量(如质量、浓度等)的改变量。某学习小组用块状纯锌和200mL稀硫酸反应研究化学反应速率,实验装置图如右图。
,rX(A)表示物质A物理量(如质量、浓度等)的改变量。某学习小组用块状纯锌和200mL稀硫酸反应研究化学反应速率,实验装置图如右图。
可选用试剂及规格:纯锌、粗锌(含铜杂质)、1mol/L 稀硫酸、2mol/L 稀硫酸,
反应温度:250C、350C
(1)请写出锌和硫酸反应的离子方程式
(2)为表达锌和硫酸反应快慢,该学习小组设计了如下表格,请填充表格丁、戊、己三处。
| 编号 | 反应速率表达式的定义 | 反应速率表达式 | 反应速率单位 |
| ① | 单位时间内H+浓度的变化量 | V(H+) = | mol / L.min |
| ② | 丁 | 戊 | 己 |
| ③ | 单位时间内生成H2标况下的体积 | V(H2) = | L / min |
(3)该学习小组选用0.1 mol Zn和200 mL 1mol/L 稀硫酸(硫酸过量)在250C反应进行研究,用秒表计时,至锌块完全溶解且溶液中不再有气泡放出时,记录反应时间为5分钟,该反应速率V(H+) =
(4)该小组对“影响反应速率的因素”进行了分析,设计如下系列实验,庚辛壬癸四处空白。
| 编号 | 锌的形状 | 锌的规格 | 硫酸的浓度 | 反应温度 | 实验设计的目的 |
| ① | 块状 | 纯锌 | 1mol/L | 250C | 实验①和②研究的目的是 庚 ;
实验②和③研究硫酸浓度对反应速率影响; 实验③和④研究锌的规格对反应速率影响;
实验④和⑤研究的目的是 癸 ;
|
| ② | 颗粒状 | 纯锌 | 1mol/L | 250C | |
| ③ | 颗粒状 | 纯锌 | 辛 | 250C | |
| ④ | 颗粒状 | 壬 | 2mol/L | 250C | |
| ⑤ | 颗粒状 | 粗锌 | 2mol/L | 350C | |
| …… |
(15分)广义的化学反应速率可以用参加化学反应的任一种物质“在单位时间内某一可测的物理量的变化量”来表示,即V(A) = 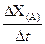 ,rX(A)表示物质A物理量(如质量、浓度等)的改变量。某学习小组用块状纯锌和200mL稀硫酸反应研究化学反应速率,实验装置图如右图。
,rX(A)表示物质A物理量(如质量、浓度等)的改变量。某学习小组用块状纯锌和200mL稀硫酸反应研究化学反应速率,实验装置图如右图。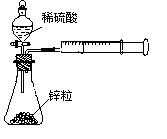
可选用试剂及规格:纯锌、粗锌(含铜杂质)、1mol/L 稀硫酸、2mol/L 稀硫酸,
反应温度:250C 、350C
(1)请写出锌和硫酸反应的离子方程式
(2)为表达锌和硫酸反应快慢,该学习小组设计了如下表格,请填充表格丁、戊、己三处。
| 编号 | 反应速率表达式的定义 | 反应速率表达式 | 反应速率单位 |
| ① | 单位时间内H+浓度的变化量 | V(H+) =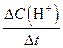 | mol / L.min |
| ② | 丁 | 戊 | 己 |
| ③ | 单位时间内生成H2标况下的体积 | V(H2) = 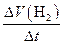 | L / min |
| 编号 | 锌的形状 | 锌的规格 | 硫酸的浓度 | 反应温度 | 实验设计的目的 |
| ① | 块状 | 纯锌 | 1mol/L | 250C | 实验①和②研究的目的是 庚 ; 实验②和③研究硫酸浓度对反应速率影响; 实验③和④研究锌的规格对反应速率影响; 实验④和⑤研究的目的是 癸 ; |
| ② | 颗粒状 | 纯锌 | 1mol/L | 250C | |
| ③ | 颗粒状 | 纯锌 | 辛 | 250C | |
| ④ | 颗粒状 | 壬 | 2mol/L | 250C | |
| ⑤ | 颗粒状 | 粗锌 | 2mol/L | 350C | |
| …… | |||||
(15分)广义的化学反应速率可以用参加化学反应的任一种物质“在单位时间内某一可测的物理量的变化量”来表示,即V(A) = 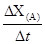 ,rX(A)表示物质A物理量(如质量、浓度等)的改变量。某学习小组用块状纯锌和200mL稀硫酸反应研究化学反应速率,实验装置图如右图。
,rX(A)表示物质A物理量(如质量、浓度等)的改变量。某学习小组用块状纯锌和200mL稀硫酸反应研究化学反应速率,实验装置图如右图。
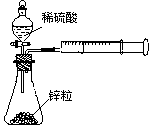
可选用试剂及规格:纯锌、粗锌(含铜杂质)、1mol/L 稀硫酸、2mol/L 稀硫酸,
反应温度:250C 、350C
(1)请写出锌和硫酸反应的离子方程式
(2)为表达锌和硫酸反应快慢,该学习小组设计了如下表格,请填充表格丁、戊、己三处。
|
编号 |
反应速率表达式的定义 |
反应速率表达式 |
反应速率单位 |
|
① |
单位时间内H+浓度的变化量 |
V(H+) = |
mol / L.min |
|
② |
丁 |
戊 |
己 |
|
③ |
单位时间内生成H2标况下的体积 |
V(H2) = |
L / min |
(3)该学习小组选用0.1 mol Zn和200 mL 1mol/L 稀硫酸(硫酸过量)在250C反应进行研究,用秒表计时,至锌块完全溶解且溶液中不再有气泡放出时,记录反应时间为5分钟,该反应速率V(H+) =
(4)该小组对“影响反应速率的因素”进行了分析,设计如下系列实验,庚辛壬癸四处空白。
|
编号 |
锌的形状 |
锌的规格 |
硫酸的浓度 |
反应温度 |
实验设计的目的 |
|
① |
块状 |
纯锌 |
1mol/L |
250C |
实验①和②研究的目的是 庚 ;
实验②和③研究硫酸浓度对反应速率影响; 实验③和④研究锌的规格对反应速率影响;
实验④和⑤研究的目的是 癸 ;
|
|
② |
颗粒状 |
纯锌 |
1mol/L |
250C |
|
|
③ |
颗粒状 |
纯锌 |
辛 |
250C |
|
|
④ |
颗粒状 |
壬 |
2mol/L |
250C |
|
|
⑤ |
颗粒状 |
粗锌 |
2mol/L |
350C |
|
|
…… |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com