
题目列表(包括答案和解析)
已知:RCH2COOH ![]()
![]()
![]() +RCl
+RCl![]()
![]() +NaCl
+NaCl
I.冠心平F是降血脂、降胆固醇的药物,它的一条合成路线如下:

⑴A为一元羧酸,8.8gA与足量NaHCO3溶液反应生成 2.24LCO2(标准状况),A的分子式为 。
⑵写出符合A分子式的所有甲酸酯的结构简式
⑶B是氯代羧酸,其核磁共振氢谱有两个峰,写出B![]() C的反应方程式: 。
C的反应方程式: 。
⑷C+E![]() F的反应类型为 。
F的反应类型为 。
⑸写出A和F的结构简式:A. ;F. 。
⑹D的苯环上有两种氢,它所含官能团的名称为 ;
写出a、b所代表的试剂:a. ;b. 。
II.按如下路线,由C可合成高聚物H:
C![]() G
G![]() H
H
⑺C![]() G的反应类型为 。
G的反应类型为 。
⑻写出G![]() H的反应方程式 。
H的反应方程式 。
某稀硫酸和稀硝酸的混合溶液200 mL,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解9.6 g 。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如下图所示(已知硝酸只被还原为NO气体)。下列 分析或结果错误的是
 | |
A.原混合酸中NO3- 物质的量为0.1 mol
B.OA段产生的是NO,AB段的反应为
Fe + 2Fe3+ = 3Fe2+, BC段产生氢气
C.第二份溶液中最终溶质为FeSO4
D.H2SO4 浓度为2.5 mol?L-1
①元素的原子序数按A、B、C、D、E依次增大,原子半径按D、E、B、C、A顺序依次减小;
②A、D同主族,A是所有元素中原子半径最小的元素;?
③B、D、E三者的最高价氧化物对应的水化物依次为甲、乙、丙,它们两两之间均可反应生成可溶性盐和水,且所得盐中均含C元素;?
④B、E两种元素原子最外层电子数之和等于A、C、D三种元素原子最外层电子数之和。
请填写下列空白:?
(1)D2C2的电子式 。?
(2)1 mol E单质与足量乙的溶液反应,能生产 mol A2气体。并写出其反应的离子方程式 。
(3)写出下列溶液反应的离子方程式:?
乙+丙: 。?
(4)化合物BA3与BC在加热和有催化剂存在的条件下能发生反应,生成两种无毒物质,其反应的化学方程式为 。?
(5)以石墨为电极,电解乙的溶液400 mL,当电路中通过a mol电子时,阴、阳两极共产生气体 L(标准状况),溶液中c(OH-) (填“增大”“减小”或“不变”)。?
①元素的原子序数按A、B、C、D、E依次增大,原子半径按D、E、B、C、A顺序依次减小;
②A、D同主族,A是所有元素中原子半径最小的元素;?
③B、D、E三者的最高价氧化物对应的水化物依次为甲、乙、丙,它们两两之间均可反应生成可溶性盐和水,且所得盐中均含C元素;?
④B、E两种元素原子最外层电子数之和等于A、C、D三种元素原子最外层电子数之和。?
请填写下列空白:?
(1)D2C2的电子式 。?
(2)1 mol E单质与足量乙的溶液反应,能生产 mol A2气体。并写出其反应的离子方程式 。
(3)写出下列溶液反应的离子方程式:?
乙+丙: 。?
(4)化合物BA3与BC在加热和有催化剂存在的条件下能发生反应,生成两种无毒物质,其反应的化学方程式为 。?
(5)以石墨为电极,电解乙的溶液400 mL,当电路中通过a mol电子时,阴、阳两极共产生气体 L(标准状况),溶液中c (OH-) (填“增大”“减小”或“不变”)。
燃料电池是一种连续的将燃料和氧化剂的化学能直接转化为电能的化学电池。氢气、烃、肼、甲醇等液体或气体,均可以作燃料电池的燃料。请回答下列问题:
(I)以甲烷和氧气为原料,氢氧化钠溶液为电解质溶液构成电池。写出其正极电极反应式 。
(II)以上述电池为电源,石墨为电极电解1L 0. 1mol/L的氯化钾溶液。回答下列问题:
(1)写出电解总反应的离子方程式 。
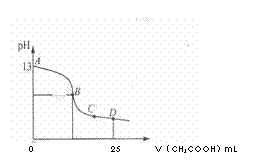
(2)室温时,电解一段时间后,取25mL上述电解后溶液,滴加0.2mol/L醋酸,加入醋酸的体积与溶液的pH的关系如图所示(不考虑能量损失和气体溶于水,溶液体积变化忽略不计)。
①计算消耗标准状况下甲烷 mL。
②若图中的B点pH=7,则酸碱恰好完全反应的点在 区间(填“AB”、“BC”或“CD”)。
③AB区间溶液中各离子浓度大小关系中可能正确的是 。
A. c(K+)>c(OH-)>c (CH3COO-) >c(H+)
B. c(K+)>c(CH3COO-)>c(OH-) >c(H+)
C. c(K+)>c(CH3COO-)=c(OH-) >c(H+)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com