
题目列表(包括答案和解析)
海洋是资源的宝库,蕴藏着丰富的化学元素,如氯、溴、碘等。
(1)在光照条件下,氯气和氢气反应过程如下:
①Cl2―→Cl+Cl ②Cl+H2―→HCl+H ③H+Cl2―→HCl+Cl ……
反应②中形成的化合物的电子式为______;反应③中被破坏的化学键属于______键(填“极性”或“非极性”)。
(2)在短周期主族元素中,氯元素及与其相邻元素的原子半径从大到小的顺序是________ (用元素符号表示)。与氯元素同周期且金属性最强的元素位于周期表的第________周期________族。
(3)卤素单质及化合物在许多性质上都存在着递变规律。下列有关说法正确的是____。
a.卤化银的颜色按AgCl、AgBr、AgI的顺序依次加深
b.卤化氢的键长按H—F、H—Cl、H—Br、H—I的顺序依次减小
c.卤化氢的还原性按HF、HCl、HBr、HI的顺序依次减弱
d.卤素单质与氢气化合按F2、Cl2、Br2、I2的顺序由难变易
(4)卤素单质的键能大小如图。由图推断:
①非金属性强的卤素,其单质分子的化学键________断裂(填“容易”或“不容易”或“不一定容易”)。
②卤素单质键能大小与键长的关系为:______________________________________。
海洋是资源的宝库,蕴藏着丰富的化学元素,如氯、溴、碘等.
(1)在光照条件下,氯气和氢气反应过程如下:
①Cl2→Cl+Cl ②Cl+H2→HCl+H ③H+Cl2→HCl+Cl……
反应②中形成的化合物的电子式为________;反应③中被破坏的化学键属
于________键(填“极性”或“非极性”).
(2)在短周期主族元素中,氯元素及与其相邻元素的原子半径从大到小的顺序是________(用元素符号表示).与氯元素同周期且金属性最强的元素位于周期表的第________周期________族.
(3)卤素单质及化合物在许多性质上都存在着递变规律.下列有关说法正确的是________.
a.卤化银的颜色按AgCl、AgBr、AgI的顺序依次加深
b.卤化氢的键长按H-F、H-C1、H-Br、H-I的顺序依次减小
c.卤化氢的还原性按HF、HCl、HBr、HI的顺序依次减弱
d.卤素单质与氢气化合按F2、Cl2、Br2、I2的顺序由难变易
(4)卤素单质的键能大小如图.由图推断:

①非金属性强的卤素,其单质分子的化学键
________断裂(填“容易”或“不容易”或“不一定容易”).②卤素单质键能大小与键长的关系为:
___________________
(1)常温下,高锰酸钾晶体遇浓盐酸会生成一种气体,该气体是由瑞典化学家舍勒首先发现的。如图所示,将浓盐酸小心滴入Y形管B端。
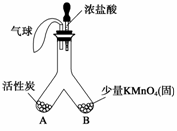
①开始观察到的现象是 。
②一段时间后又可观察到 ,请解释这一现象 。
③应用活性炭的此性质可制作 来达到防毒、防臭的目的(举一例即可)。
(2)①写出CO2和Na2O2反应的化学方程式 。
②某学生判断SO2和Na2O2反应能生成硫酸钠,你认为他的判断合理吗? 。
简要说明理由: 。
③该同学无法断定反应中是否有氧气生成,拟使用如图所示装置进行实验(图中铁架台等装置已略去)。

装置中B的作用是 ,
D的作用是 。
④如何证明该同学的两个推断?
。
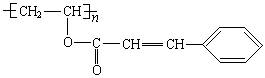
感光性高分子也称为“光敏哇高分子”,是一种在彩电荧光屏及大规模集成电路制造中应用较广的新型高分子材料,其结构简式为 ,试回答下列问题:
,试回答下列问题:
(1)已知它是由两种单体经酯化和聚合而成的,试推断这两种单体的结构简式________,________________。
(2)写出在(1)中由两种单体生成高聚物的化学反应方程式________________。
(3)对此高聚物的性质判断不正确的是( )
A.在酸性条件下可以发生水解
B.此高聚物不能使溴水褪色
C.此高聚物可以使酸性高锰酸钾溶液褪色
D.此高聚物可与液溴发生取代反应
E.此高聚物水解后可得到另外一种高聚物
 ,试回答下列问题:
,试回答下列问题:
(1)已知它是由两种单体经酯化和聚合而成的,试推断这两种单体的结构简式________,________________。
(2)写出在(1)中由两种单体生成高聚物的化学反应方程式________________。
(3)对此高聚物的性质判断不正确的是( )
A.在酸性条件下可以发生水解
B.此高聚物不能使溴水褪色
C.此高聚物可以使酸性高锰酸钾溶液褪色
D.此高聚物可与液溴发生取代反应
E.此高聚物水解后可得到另外一种高聚物
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com