
题目列表(包括答案和解析)
已知某氯代烃A的相对分子质量为113,且氯的质量分数是62.8%,A进行核磁共振氢谱分析,谱图中只有两组峰。
(1)A的分子式是_________________________
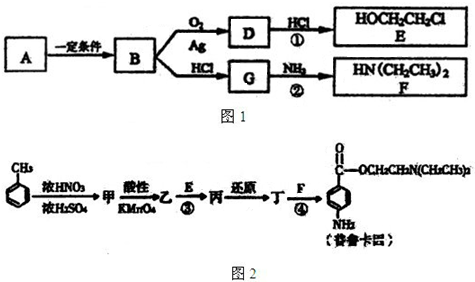
(2)A有如下的转化关系: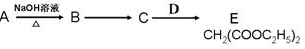
①C中的官能团名称是______________;C可以发生的反应有________________。
a.与氢气加成 b.缩聚反应 c.中和反应 d.水解反应 e.取代反应②D的结构简式为:________________。
(3)巴比妥是一类重要的有机物,其中一些常常可用作镇静和催眠的药物,其结构简式如右图所示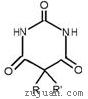 ,R、R’为烃基或氢原子。下图是由E合成一种巴比妥H和一种重要有机中间体环戊甲酸(I)的流程:
,R、R’为烃基或氢原子。下图是由E合成一种巴比妥H和一种重要有机中间体环戊甲酸(I)的流程:
已知:

①写出E转化为F的化学方程式:___________________________。
②巴比妥H的结构简式是_____________________________。
③I有多种同分异构体,其中满足:i属于甲酸酯;ii能使溴的四氯化碳溶液褪色;iii结构中只有一个甲基的共有________种,写出其中任意一种:_________________。
(4)尿素(H2N-CO-NH2)也可与甲醛合成脲甲醛树脂,其可用于耐水性和介电性能要求不高的制品,如插线板、日用品、装饰品,也可用于部分餐具的制造。反应过程如下:
第一步生成聚合前体:
酸性条件:H2N-CO-NH2 + 2HCHO 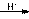 HOCH2NH-CO-NHCH2OH
HOCH2NH-CO-NHCH2OH
碱性条件:H2N-CO-NH2 + 4HCHO  (HOCH2)2N-CO-N(CH2OH)2
(HOCH2)2N-CO-N(CH2OH)2
第二步聚合:
第一步反应得到的聚合前体继续在酸性或碱性条件下发生缩聚反应。
①第一步生成聚合前体的反应属于_________反应;要得到体型的脲甲醛树脂,尿素与甲醛需要在_________(填“酸性”或“碱性”)条件下反应。
②写出由酸性条件下得到的聚合前体通过醚键缩聚得到脲甲醛树脂的化学方程式:
____________________________________________________________________________。
 A、B、C、D、E、F六种元素分属三个短周期,且原子序数依次增大,A的原子在周期表中半 径最小,A、D伺主族,可形成离子化合物DA;C、F同主族,可形成FC2,FC3两种分子B,D,E 三者的最高价氧化物对应的水化物两两之间均可反应生成可溶性盐和水,所得盐中均含C元 素.请填写下列空白:
A、B、C、D、E、F六种元素分属三个短周期,且原子序数依次增大,A的原子在周期表中半 径最小,A、D伺主族,可形成离子化合物DA;C、F同主族,可形成FC2,FC3两种分子B,D,E 三者的最高价氧化物对应的水化物两两之间均可反应生成可溶性盐和水,所得盐中均含C元 素.请填写下列空白: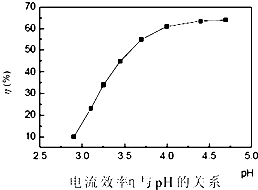 人造金刚石酸洗废液中含有大量的Ni2+、Mn2+、Co2+等离子.某厂技术人员设计了如下方案,使上述离子的浓度降低到排放标准,且得到了纯度较高的镍粉.
人造金刚石酸洗废液中含有大量的Ni2+、Mn2+、Co2+等离子.某厂技术人员设计了如下方案,使上述离子的浓度降低到排放标准,且得到了纯度较高的镍粉.| 金属元素 | Ni | Mn | Co | Fe | Cu | Zn |
| 浓度(g?L-1) | 45 | 15 | 7.5 | ≤0.1 | ≤0.05 | ≤0.05 |
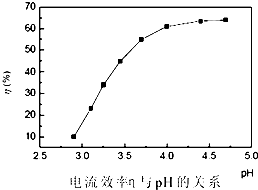 人造金刚石酸洗废液中含有大量的Ni2+、Mn2+、Co2+等离子.某厂技术人员设计了如下方案,使上述离子的浓度降低到排放标准,且得到了纯度较高的镍粉.
人造金刚石酸洗废液中含有大量的Ni2+、Mn2+、Co2+等离子.某厂技术人员设计了如下方案,使上述离子的浓度降低到排放标准,且得到了纯度较高的镍粉.| 金属元素 | Ni | Mn | Co | Fe | Cu | Zn |
| 浓度(g?L-1) | 45 | 15 | 7.5 | ≤0.1 | ≤0.05 | ≤0.05 |
| 浓硫酸 |
| 浓硫酸 |


 ):
):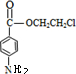

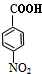 +HOCH2CH2Cl
+HOCH2CH2Cl| 浓硫酸 |
| △ |
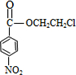 +H2O
+H2O +HOCH2CH2Cl
+HOCH2CH2Cl| 浓硫酸 |
| △ |
 +H2O
+H2O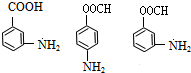

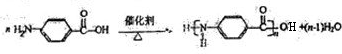
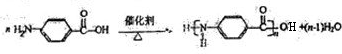
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com