
题目列表(包括答案和解析)
下图是中学化学某些物质之间在一定条件下的相互转化关系,已知A是一种常见的液态化合物, C、D、G、H、K是单质,其它为化合物,G、K是普通钢中的两种重要元素,其中K含量少,E、F对应溶液的酸碱性相反,F的焰色反应为黄色,请按要求作答:
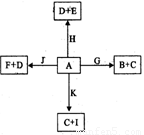
(1)写出化合物J的电子式:_______________。
(2)G3+比G2+的稳定性的原因 ,组成D、H、K三种元素的第一电离能由大到小的顺序为 (写元素符号)。A分子中心原子的杂化方式为 ,A可与Cu2+形成天蓝色的物质,画出该离子的结构示意图 ,写出一种与化合物I 为等电子体关系的阴离子
(3)B与足量稀硝酸反应,当参加反应的硝酸为4mol,转移电子的物质的量为 _________mol(保留2位有效数字)。
(4)已知在200℃,101Kpa下,0.12g单质K与A完全反应生成C与I,吸收了1316 J的能量,写出此反应的热化学方程式:_________________________。
(5)①以Pt为电极,由I、D以及F的溶液组成原电池,则负极的电极反应为:___________。
②若用此电池电解300mL 5mol/L的氯化钠溶液一段时间,两极均收集到标准状况下3.36L气体,此时溶液的pH为_________(假设电解前后溶液体积不变化)。
③若往该电解后所得溶液中通入二氧化碳气体4.48L(标准状况),此时溶液中所有离子浓度的关系由大到小的顺序为:_______________________
下图是中学化学某些物质之间在一定条件下的相互转化关系,已知A是一种常见的液态化合物,C、D、G、H、K是单质,其它为化合物,G、K是普通钢中的两种重要元素,其中K含量少,E、F对应溶液的酸碱性相反,F的焰色反应为黄色,请按要求作答:
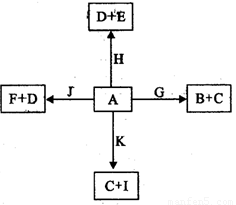
(1)写出化合物的电子式:_________________________。
(2)①写出A与J反应的离子方程式:_______________________________________。
②将少量的H通入F的溶液中,反应的总离子方程式为:_________________________。
(3)B与足量稀硝酸反应,当参加反应的硝酸为4mol,转移电子的物质的量为_________mol(保留2位有效数字)。
(4)已知在200℃,101Kpa下,0.12g单质K与A完全反应生成C与I,吸收了1316J的能量,写出此反应的热化学方程式:_________________________________________。
(5)①以Pt为电极,由I、D以及F的溶液组成原电池,则正极的电极反应为:___________。
②若用此电池电解300mL5mol/L的氯化钠溶液一段时间,两极均收集到标准状况下3.36L气体,此时溶液的pH为_________(假设电解前后溶液体积不变化)。
③若往该电解后所得溶液中通入二氧化碳气体4.48L(标准状况),此时溶液中所有离子浓度的关系由大到小的顺序为:_______________________________________。
下图是中学化学某些物质之间在一定条件下的相互转化关系,已知A是一种常见的液态化合物,C、D、G、H、K是单质,其它为化合物,G、K是普通钢中的两种重要元素,其中K含量少,E、F对应溶液的酸碱性相反,F的焰色反应为黄色,请按要求作答: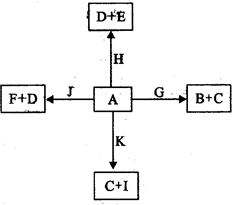
(1)写出化合物的电子式:_________________________。
(2)①写出A与J反应的离子方程式:_______________________________________。
②将少量的H通入F的溶液中,反应的总离子方程式为:_________________________。
(3)B与足量稀硝酸反应,当参加反应的硝酸为4mol,转移电子的物质的量为_________mol(保留2位有效数字)。
(4)已知在200℃,101Kpa下,0.12g单质K与A完全反应生成C与I,吸收了1316J的能量,写出此反应的热化学方程式:_________________________________________。
(5)①以Pt为电极,由I、D以及F的溶液组成原电池,则正极的电极反应为:___________。
②若用此电池电解300mL5mol/L的氯化钠溶液一段时间,两极均收集到标准状况下3.36L气体,此时溶液的pH为_________(假设电解前后溶液体积不变化)。
③若往该电解后所得溶液中通入二氧化碳气体4.48L(标准状况),此时溶液中所有离子浓度的关系由大到小的顺序为:_______________________________________。
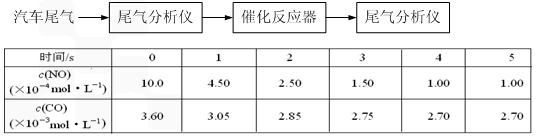

下图表示一些常见物质间的相互转换关系,其中C、E都是金属单质,常温下H为无色液体,C与B的稀溶液不反应,B与K是同一类别的物质,在无色灯焰中灼烧F和L时火焰均为黄色.将新制M的悬浊液与病人尿液共热,能诊断病人是否患有糖尿病.试回答:
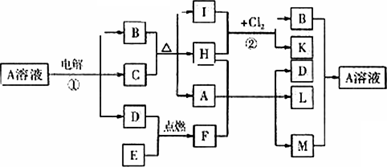
(1)F的电子式为________;反应①的阳极反应式为________.
(2)反应②的化学方程式为________.
(3)B溶液与M反应的离子方程式为________.
(4)I与F有一项相同的用途是________.
(5)新制M的悬浊液与葡萄糖共热至沸腾,发生反应的化学方程式为________.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com