
题目列表(包括答案和解析)
(本题10分)下面是以化合物I为原料合成一种香精.(化合物VI)的合成路线,反应在一定条件下进行。化合物Ⅵ广泛用于香精的调香剂。
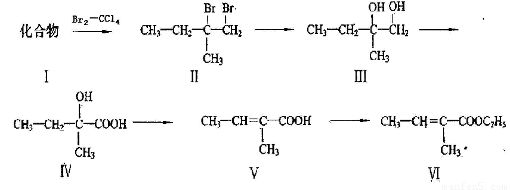
回答下列问题:
(1)化合物I生成化合物Ⅱ的反应原子利用率可达100%,化合物I的结构简式为
。
(2)写出化合物V合成化合物Ⅵ的反应方程式
(3)写出一种可鉴别化合物Ⅲ和Ⅳ的化学试剂:
(4)化合物V的多种同分异构体中,与化合物V官能团种类相同且无支链的共有 种。 (5)化合物Ⅵ不能发生的反应类型是
A.加成反应 B.酯化反应
C.水解反应 D.加聚反应
(本题10分)
为探究乙烯与溴的加成反应,甲同学设计并进行了如下实验:先用乙醇和浓硫酸为原料制取乙烯(CH3CH2OH浓硫酸170 ℃CH2===CH2+H2O),将生成的气体直接通入溴水中,发现溴水褪色,即证明乙烯与溴水发生了加成反应。乙同学发现在甲同学的实验中,产生的气体有刺激性气味,推测在制得的乙烯中还可能含有少量有还原性的杂质气体,由此他提出必须先把杂质气体除去,再与溴水反应。
(1)甲同学设计的实验________(填“能”或“不能”)验证乙烯与溴水发生了加成反应,其理由是________(填编号)。
A.使溴水褪色的反应,未必是加成反应
B.使溴水褪色的反应,就是加成反应
C.使溴水褪色的气体,未必是乙烯
D.使溴水褪色的气体,就是乙烯
(2)乙同学推测此乙烯中可能含有的一种杂质气体是____________,它与溴水发生反应的化学方程式是___________________,在验证过程中必须全部除去。
(3)为了验证乙烯与溴水的反应是加成反应而不是取代反应,可采取哪些方法?
(本题10分)
为探究乙烯与溴的加成反应,甲同学设计并进行了如下实验:先用乙醇和浓硫酸为原料制取乙烯(CH3CH2OH浓硫酸170 ℃CH2===CH2+H2O),将生成的气体直接通入溴水中,发现溴水褪色,即证明乙烯与溴水发生了加成反应。乙同学发现在甲同学的实验中,产生的气体有刺激性气味,推测在制得的乙烯中还可能含有少量有还原性的 杂质气体,由此他提出必须先把杂质气体除去,再与溴水反应。
杂质气体,由此他提出必须先把杂质气体除去,再与溴水反应。
(1)甲同学设计的实验________(填“能”或“不能”)验证乙烯与溴水发生了加成反应,其理由是________(填编号)。
| A.使溴水褪色的反应,未必是加成反应 |
| B.使溴水褪色的反应,就是加成反应 |
| C.使溴水褪色的气体,未必是乙烯 |
| D.使溴水褪色的气体,就是乙烯 |
(本题10分)
为探究乙烯与溴的加成反应,甲同学设计并进行了如下实验:先用乙醇和浓硫酸为原料制取乙烯(CH3CH2OH浓硫酸170 ℃CH2===CH2+H2O),将生成的气体直接通入溴水中,发现溴水褪色,即证明乙烯与溴水发生了加成反应。乙同学发现在甲同学的实验中,产生的气体有刺激性气味,推测在制得的乙烯中还可能含有少量有还原性的杂质气体,由此他提出必须先把杂质气体除去,再与溴水反应。
(1)甲同学设计的实验________(填“能”或“不能”)验证乙烯与溴水发生了加成反应,其理由是________(填编号)。
A.使溴水褪色的反应,未必是加成反应
B.使溴水褪色的反应,就是加成反应
C.使溴水褪色的气体,未必是乙烯
D.使溴水褪色的气体,就是乙烯
(2)乙同学推测此乙烯中可能含有的一种杂质气体是____________,它与溴水发生反应的化学方程式是___________________,在验证过程中必须全部除去。
(3)为了验证乙烯与溴水的反应是加成反应而不是取代反应,可采取哪些方法?
(本题10分) A、B、C、D是四种短周期元素,它们的原子序数依次增大,其中A元素的原子只有一个电子层,又知A与C、B与D分别是同一主族元素,B、D两元素的原子核中质子数之和是A、C两元素原子核中质子数之和的二倍,又知四种元素的单质常温常压下有两种气体、两种固体。请回答下列问题:
(1)由A、B两种元素可形成E、F两种化合物,写出其中一种化合物分解生成另一种化合物的化学方程式__________________________。反应物的电子式 其所含化学键为 (a.离子键 b.极性共价键 c.非极性共价键)
(2)B元素比D元素的非金属性强的依据是: 。
①两元素组成的化合物中D元素为正价 ②单质的熔沸点的高低
③最高价氧化物对应的水化物的酸性强弱 ④气态氢化物的稳定性
(3)由A、B、D三种元素中的两种可分别形成甲、乙两种粒子,它们均为负一价双原子核的阴离子,且甲含有18个电子,乙含有10个电子,则甲与乙反应的离子方程式_________________________________________________________。
(4)写出C和D两元素的最高价氧化物对应的水化物在稀溶液里相互反应的热化学方程式(已知此反应生成1molH2O时放出的热量为57.3KJ)_____________________________________________________________________
(5)用A元素的单质与B元素的单质可以制成电池,电池中装有KOH浓溶液,用多孔的金属惰性电极浸入KOH溶液,在M极通入A的单质,N极通入B的单质,则M极是该电池的________极;N极的电极反应式为:________________________。
由此给我们的启示:在能量电池的设计上,对化学反应的要求是:
①
② 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com