œ÷¥ζ…γΜα÷–Ά≠‘ΎΒγΤχΓΔΫΜΆ®ΓΔΜζ–ΒΚΆ“±ΫπΓΔΡή‘¥ΦΑ ·Μ·ΙΛ“ΒΓΔΗΏΩΤΦΦΒ»Νλ”ρ”–ΙψΖΚΒΡ”Π”ΟΘ°Ρ≥Ά≠Ωσ ·Κ§―θΜ·Ά≠ΓΔ―θΜ·―«Ά≠ΓΔ»ΐ―θΜ·ΕΰΧζΚΆ¬ω ·Θ®SiO
2Θ©Θ§œ÷≤…”ΟΥαΫΰΖ®¥”Ωσ ·÷–Χα»ΓΆ≠Θ§ΤδΙΛ“’Νς≥ΧΆΦ»γœ¬Θ°Τδ÷–Ά≠ΒΡίΆ»ΓΘ®Ά≠¥”Υ°≤ψΫχ»κ”–Μζ≤ψΒΡΙΐ≥ΧΘ©ΚΆΖ¥ίΆ»ΓΘ®Ά≠¥””–Μζ≤ψΫχ»κΥ°≤ψΒΡΙΐ≥ΧΘ© «œ÷¥ζ ΣΖ®ΝΕΆ≠ΒΡ÷Ί“ΣΙΛ“’ ÷ΕΈΘ°
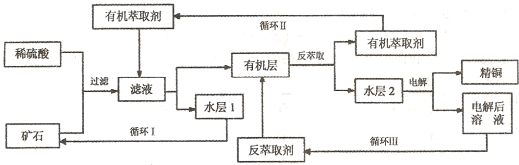
“―÷ΣΘΚΔΌCu
2O+2H
+=Cu
2++Cu+H
2OΘΜΔΎΒ±Ωσ ·÷–»ΐ―θΜ·ΕΰΧζΚ§ΝΩΧΪΒΆ ±Θ§Ω…”ΟΝρΥαΚΆΝρΥαΧζΒΡΜλΚœ“ΚΫΰ≥ωΆ≠ΘΜΔέΖ¥ίΆ»ΓΚσΒΡΥ°≤ψ2 «ΝρΥαΆ≠»ή“ΚΘ°ΜΊ¥πœ¬Ν–Έ ΧβΘΚ
Θ®1Θ©Ωσ ·”ΟœΓΝρΥα¥ΠάμΙΐ≥Χ÷–ΖΔ…ζΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΈΣΘΚCu
2O+2H
+=Cu
2++Cu+H
2O
CuO+2H+®TCu2++H2O
CuO+2H+®TCu2++H2O
ΓΔ
Fe2O3+6H+®T2Fe3++3H2OΘ§Cu+2Fe3++2Fe2++Cu2+Θ§
Fe2O3+6H+®T2Fe3++3H2OΘ§Cu+2Fe3++2Fe2++Cu2+Θ§
Θ®2Θ©ΓΑ―≠ΜΖIΓ±Ψ≠Εύ¥Έ―≠ΜΖΚσΒΡΥ°≤ψ1≤ΜΡήΦΧ–χ―≠ΜΖ Ι”ΟΘ§ΒΪΩ…Ζ÷άκ≥ω“Μ÷÷÷Ί“ΣΒΡΝρΥα―ΈΨßΧεΘ°»τΥ°≤ψ1±©¬Ε‘ΎΩ’Τχ÷–“ΜΕΈ ±ΦδΚσΘ§Ω…“‘ΒΟΒΫΝμ“Μ÷÷÷Ί“ΣΒΡΝρΥα―ΈΘ§–¥≥ωΥ°≤ψl±©¬Ε‘ΎΩ’Τχ÷–ΖΔ…ζΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ Ϋ
4Fe2++O2+4H+=4Fe3++2H2O
4Fe2++O2+4H+=4Fe3++2H2O
Θ°
Θ®3Θ©ΓΑ―≠ΜΖnΓ±÷–ίΆ»ΓΦΝ «“Μάύ≥ΤΉςΈΣκΩάύΒΡ”–ΜζΜ·ΚœΈοΘ§»γN“Μ510ΓΔN“Μ530Β»Θ°Ρ≥κΩάύΜ·ΚœΈοAΒΡΖ÷Ή”ΫαΙΙ÷–ΫωΚ§n
1Ηω-CH
3ΓΔn
2Ηω-OHΚΆn
3Ηω
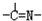
»ΐ÷÷ΜυΆ≈Θ§ΈόΜΖΉ¥ΫαΙΙΘ§»ΐ÷÷ΜυΆ≈ΒΡ ΐΡΩΙΊœΒΈΣn
3=
n1+n2-2
n1+n2-2
Θ°»τAΒΡœύΕ‘Ζ÷Ή”÷ ΝΩΈΣ116Θ§…œ ωΜυΆ≈Ν§Ϋ” ±ΧΦ‘≠Ή”ΗζΧΦ‘≠Ή”œύΝ§Θ§‘ρAΒΡΫαΙΙΦρ Ϋ «
Θ®4Θ©–¥≥ωΒγΫβΙΐ≥Χ÷–―τΦΪΘ®Εη–‘ΒγΦΪΘ©ΖΔ…ζΖ¥”ΠΒΡΒγΦΪΖ¥”Π Ϋ
4OH--4e-=2H2O+O2
4OH--4e-=2H2O+O2
Θ®5Θ©ΗΟΙΛ“’Ήν¥σΝΝΒψ «ΥϋΖϊΚœœ¬Ν–‘≠άμ
B
B
Θ°
AΘ°Μ·―ßΤΫΚβ BΘ°¬Χ…ΪΜ·―ß CΘ°÷ ΝΩ ΊΚψ DΘ°ΡήΝΩ ΊΚψ EΘ°œύΥΤœύ»ή FΘ°ΥαΦν÷–ΚΆ GΘ°―θΜ·ΜΙ‘≠Ζ¥”Π
Θ®6Θ©Ά≠ΓΔ“χΓΔΫπ «»Υάύ»œ ΕΉν‘γΒΡ»ΐ÷÷Ϋπ τΘ§“ρΈΣΚή‘γΨΆ±Μ»ΥΟ«”ΟΉς«°±“Θ§“ρΕχ”–ΓΑΜ豓Ϋπ τΓ±÷°≥ΤΘ°”…”ΎΧζΒΡΫπ τ–‘±»Ά≠ΓΔ“χΓΔΫπ«ΩΘ§œύΕ‘Εχ―‘Θ§»Υάύ»œ ΕΧζ…‘ΆμΘ°Ρ≥―–ΨΩ–‘―ßœΑ–ΓΉιΈΣΝΥ÷ΛΟςΧζΒΡΫπ τΜνΕ·–‘±»Ά≠«ΩΘ§Υϊ…ηΦΤΝΥ»γœ¬ΖΫΑΗΘΚ
ΔΌΧζΤ§÷Ο”ΎΝρΥαΆ≠»ή“Κ÷–”–Ά≠Έω≥ωΘΜ
ΔΎΧζΓΔΆ≠ΚΆ¬»ΤχΖ¥”ΠΖ÷±π…ζ≥…FeCl
3ΚΆCuCl
2ΘΜ
ΔέΉψΝΩΒΡΧζΖέΚΆΆ≠ΖέΚΆ≈®ΝρΥαΖ¥”Π…ζ≥…FeSO
4ΚΆCuSO
4ΘΜ
ΔήΆ≠Τ§÷Ο”ΎFeCl
3»ή“Κ÷–Ά≠Τ§÷πΫΞ»ήΫβΘΜ
ΔίΑ―ΧζΤ§ΚΆΆ≠Τ§÷Ο”Ύ Δ”–œΓΝρΥαΒΡ…’±≠÷–Θ§ΫΜ”ΟΒΦœΏΝ§Ϋ”Θ§ΧζΤ§…œΈόΤχ≈ί≤ζ…ζΘ§ΕχΆ≠Τ§…œ”–Τχ≈ί≤ζ…ζΘΜ
ΔόΑ―ΧζΤ§ΚΆΆ≠Τ§÷Ο”Ύ Δ”–≈®œθΥαΒΡ…’±≠÷–Θ§≤Δ”ΟΒΦœΏΝ§Ϋ”Θ§ΧζΤ§…œ”–Τχ≈ί≤ζ…ζΘ§ΕχΆ≠Τ§…œΈόΤχ≈ί≤ζ…ζΘ°
“‘…œ…ηΦΤΚœάμΒΡ”–
A
A
Θ°
AΘ°ΝΫ÷÷ΖΫΑΗ BΘ°»ΐ÷÷ΖΫΑΗ CΘ°ΥΡ÷÷ΖΫΑΗ DΘ°Έε÷÷ΖΫΑΗΘ°

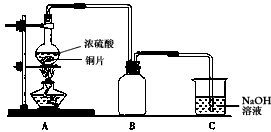
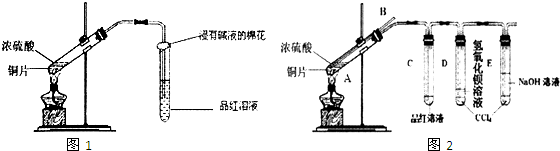
 ―–ΨΩ–‘―ßœΑ–ΓΉιΈΣΧΫΨΩCu”κ≈®H2SO4Ζ¥”ΠΦΑΤδ≤ζΈοSO2ΒΡ–‘÷ Θ§…ηΦΤ»γœ¬ Β―ιΉΑ÷ΟΘΚ
―–ΨΩ–‘―ßœΑ–ΓΉιΈΣΧΫΨΩCu”κ≈®H2SO4Ζ¥”ΠΦΑΤδ≤ζΈοSO2ΒΡ–‘÷ Θ§…ηΦΤ»γœ¬ Β―ιΉΑ÷ΟΘΚ
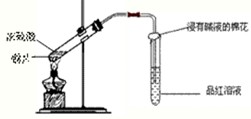 ―–ΨΩ–‘―ßœΑ–ΓΉιΈΣΧΫΨΩCu”κ≈®H2SO4Ζ¥”ΠΦΑΤδ≤ζΈοSO2ΒΡ–‘÷ Θ§…ηΦΤ»γœ¬ Β―ιΉΑ÷ΟΘΚ
―–ΨΩ–‘―ßœΑ–ΓΉιΈΣΧΫΨΩCu”κ≈®H2SO4Ζ¥”ΠΦΑΤδ≤ζΈοSO2ΒΡ–‘÷ Θ§…ηΦΤ»γœ¬ Β―ιΉΑ÷ΟΘΚ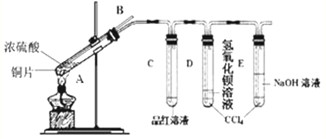

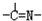 »ΐ÷÷ΜυΆ≈Θ§ΈόΜΖΉ¥ΫαΙΙΘ§»ΐ÷÷ΜυΆ≈ΒΡ ΐΡΩΙΊœΒΈΣn3=
»ΐ÷÷ΜυΆ≈Θ§ΈόΜΖΉ¥ΫαΙΙΘ§»ΐ÷÷ΜυΆ≈ΒΡ ΐΡΩΙΊœΒΈΣn3=
