
题目列表(包括答案和解析)
下列说法正确的是:
①Cl-的结构示意图 ;
;
②羟基的电子式: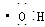 ;
;
③HClO的结构式:H—Cl—O;
④NaHCO3在水中的电离方程式:NaHCO3=Na++H++CO32-;
⑤Na2O的水溶液能导电,这不能说明Na2O是电解质;
⑥SiO2既能与氢氟酸反应又能与NaOH溶液反应,故SiO2是两性氧化物;
⑦分馏、干馏、裂化都是化学变化( )
A.①②⑤ B.①④⑥⑦ C.②③④⑥ D.②③⑤⑥⑦
下列说法正确的是:
①Cl-的结构示意图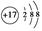 ;
;
②羟基的电子式: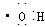 ;
;
③HClO的结构式:H—Cl—O;
④NaHCO3在水中的电离方程式:NaHCO3=Na++H++CO32-;
⑤Na2O的水溶液能导电,这不能说明Na2O是电解质;
⑥SiO2既能与氢氟酸反应又能与NaOH溶液反应,故SiO2是两性氧化物;
⑦分馏、干馏、裂化都是化学变化( )
| A.①②⑤ | B.①④⑥⑦ | C.②③④⑥ | D.②③⑤⑥⑦ |
常温下,对于下列电解质溶液,说法正确的是( )
| A.pH=1的溶液中,Fe3+、I-、NO3-、K+可以大量共存 |
B.在c(SO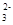 )=0.1 mol·L-1的溶液中,Na+、Cl-、H+、Ca2+可以大量共存 )=0.1 mol·L-1的溶液中,Na+、Cl-、H+、Ca2+可以大量共存 |
| C.工业上用过量的NaOH溶液吸收SO2:SO2 + OH- ="=" HSO3- |
| D.将AlCl3溶液滴入NaOH溶液中反应的离子方程式:Al3+ + 4OH- = AlO2- + 2H2O |
下列关于电解质溶液的叙述正确的是
A.常温下,pH=7的NH4Cl与氨水的混合溶液中离子浓度大小顺序为、c(Cl-)>c(NH4+)>c(H+)>c(OH-)
B.10mL0.1mol/LNH4Cl溶液5mL0.2mol/L NaOH溶液混合:c(Na+)=c(Cl-)>c(OH-)>c(H+)
C.相同温度和浓度的钾盐溶液中,酸式盐的pH一定小于正盐的pH
D.常温下,同浓度的Na2S与NaHS溶液相比,Na2S溶液的pH大
下列关于电解质溶液的叙述正确的是
| A.常温下,pH=7的NH4Cl与氨水的混合溶液中离子浓度大小顺序为、c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| B.10mL0.1mol/LNH4Cl溶液5mL0.2mol/L NaOH溶液混合:c(Na+)=c(Cl-)>c(OH-)>c(H+) |
C.相同温度和浓度的钾盐溶液中,酸式盐的p H一定小于正盐的pH H一定小于正盐的pH |
| D.常温下,同浓度的Na2S与NaHS溶液相比,Na2S溶液的pH大 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com