
题目列表(包括答案和解析)
在一定条件下,进入氨合成塔的混合气体中含![]() 的体积分数为22%,含
的体积分数为22%,含![]() 的体积分数为78%,经过合成反应达到平衡后,在相同的温度和压强下,气体的体积缩小至原体积的95%,
的体积分数为78%,经过合成反应达到平衡后,在相同的温度和压强下,气体的体积缩小至原体积的95%,![]() 的转化率与下面接近的数值是
的转化率与下面接近的数值是
[ ]
在一定条件下,进入氨合成塔的混合气体中含![]() 的体积分数为22%,含
的体积分数为22%,含![]() 的体积分数为78%,经过合成反应达到平衡后,在相同的温度和压强下,气体的体积缩小至原体积的95%,
的体积分数为78%,经过合成反应达到平衡后,在相同的温度和压强下,气体的体积缩小至原体积的95%,![]() 的转化率与下面接近的数值是
的转化率与下面接近的数值是
[ ]
|
在一定条件下,进入氨合成塔的混合气体中氮气的体积占22%,氢气的体积占78%,经合成反应达到平衡后,在相同温度和压强下,气体体积缩小至原体积的95%,氮气的转化率接近于 | |
| [ ] | |
A. |
11.5% |
B. |
10.5% |
C. |
9.75% |
D. |
13.2% |
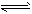 CH3OH(g)+H2O(g) △H=-49.0kJ/mol 测得CO2和
CH3OH(g)+H2O(g) △H=-49.0kJ/mol 测得CO2和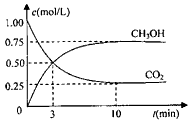
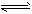 2NH3(g) △H=-92 kJ·mol-1。
2NH3(g) △H=-92 kJ·mol-1。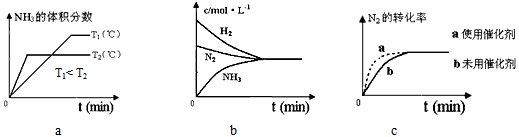
氨是一种重要的基础化工原料,可以生产硝酸等一系列化工产品。德国人哈伯在1905年发明的合成氨反应原理为:
![]()
![]() ;
;![]()
回答下列问题:
(1)将10mol ![]() 和30mol
和30mol ![]() 装入密闭容器中,在一定条件下反应达到平衡,若有15%的
装入密闭容器中,在一定条件下反应达到平衡,若有15%的![]() 转化,则反应放出的热量是_______________kJ。
转化,则反应放出的热量是_______________kJ。
(2)工业合成氨生产中采取的措施是____________(填序号)
A. 采用较低压强
B. 采用700K左右的高温
C. 用铁触媒作催化剂
D. 将氨液化及时从混合物中分离,![]() 循环到合成塔中,并补充
循环到合成塔中,并补充![]()
(3)用下图所示装置(夹持固定装置已略去)在实验室中模拟工业制![]()

回答下列问题:
①实验时,A装置中盛放的试剂是__________________________;
装置B中反应的化学方程式为_______________________________________;
②C装置中盛放的试剂是_______________________________________;
该物质的主要作用是_______________________________________;
D装置的作用是_______________________________________;
③若将上图所示装置中虚线部分换成下图所示装置进行实验。反应开始前,分液漏斗中盛放的药品是______________________;烧瓶中盛放的药品是_____________________。

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com