Ⅰ.玻璃棒是中学化学实验中常用的仪器.下列实验过程中,一般不需要用玻璃棒的是
______(填写编号)
①用pH试纸测定Na
2CO
3溶液的pH; ②配制一定物质的量浓度的氯化钠溶液; ③将适量氯化铁饱和溶液滴入沸水中制备氢氧化铁胶体; ④探究Ba(OH)
28H
2O晶体和NH
4Cl晶体反应过程中的能量变化; ⑤用蒸馏法分离两种沸点差距较大的液体; ⑥过滤分离互不相溶的固体和液体; ⑦用已知浓度的盐酸滴定待测浓度的NaOH溶液的酸碱中和滴定过程; ⑧稀释浓H
2SO
4的过程
Ⅱ.为测定某含有杂质Na
2O的Na
2O
2样品的纯度,某小组同学分别设计了如下方案.
方案一准确称量样品mg,与水充分反应后将溶液的体积稀释为VmL,从中取出V
1mL溶液,装入锥形瓶,用已知浓度的盐酸进行滴定,以确定溶液的浓度,再计算出样品中Na
2O
2的含量.
(1)此方案中,酸碱中和滴定时应选用指示剂是______.
方案二准确称量样品mg,将样品与二氧化碳充分反应,通过测定反应产生氧气的体积,计算出样品中Na
2O
2的含量.
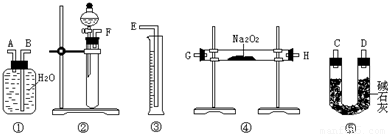
(2)该方案的实验过程中,仪器的连接顺序是______(填仪器下方序号),①中的进气口为______(填“A”或“B”)
(3)装置⑤的作用是______.
(4)在可供选用的反应物只有CaCO3固体,6mol/L盐酸和蒸馏水时,请设计一种最简单的测定Na
2O
2纯度的实验方案______.



