
题目列表(包括答案和解析)
化学与科学、技术、社会、环境密切相关。下列说法中,你认为正确的是( )
①加热能杀死甲型 H1N1 流感病毒是因为病毒的蛋白质受热变性
②可用铝制容器存放浓硝酸,是因为常温下浓硝酸与铝不反应
③光缆在信息产业中有广泛应用,制造光缆的主要材料是单质硅
④结构陶瓷碳化硼(B4C3)常用于制造切削工具,它是一种新型无机非金属材料,属于原子晶体
⑤金刚石是自然界中硬度最大的物质,不可能与氧气发生反应
⑥玻璃、水泥的生产都要用石灰石做原料
⑦Na2O2可用于呼吸面具中作为氧气的来源
| A.①⑤⑦ | B.④⑥⑦ | C.②③⑤ | D.③④⑥ |
| X的基态原子中电子分布在三个不同的能级中,且每个能级的电子总数相同 |
| Y元素的气态氢化物与其最高价氧化物对应的水化物能发生化学反应 |
| Z元素的族序数是周期数的三倍 |
| W原子的第一至第六电离能分别为:I1=578kJ?mol-1,I2=1817kJ?mol-1, I3=2745kJ?mol-1,I4=11575kJ?mol-1,I5=14830kJ?mol-1,I6=18376kJ?mol-1 |
| Q为前四周期中电负性最小的元素 |
| R位于周期表的第11列 |
 或
或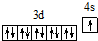
 或
或




湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com