
题目列表(包括答案和解析)
 (11分)不久前,美国威斯康星洲Emory大学的研究者们发现了一种可以在温和条件下将硫醚(普通醚的氧原子被硫代替)选择性地氧化为硫氧化物的水溶性催化剂。新催化剂是金(III)配合物(如图),催化速度比已知以氧气为氧化剂的高温水溶性催化剂高几个数量级。该发现的潜在应用价值是可以在空气中分解掉化妆品、涂料、织物的污染物。回答下列问题:
(11分)不久前,美国威斯康星洲Emory大学的研究者们发现了一种可以在温和条件下将硫醚(普通醚的氧原子被硫代替)选择性地氧化为硫氧化物的水溶性催化剂。新催化剂是金(III)配合物(如图),催化速度比已知以氧气为氧化剂的高温水溶性催化剂高几个数量级。该发现的潜在应用价值是可以在空气中分解掉化妆品、涂料、织物的污染物。回答下列问题:
5-1 下列物质中属于硫醚的有( )。
A.CH3-SH B.CH3-S-CH3 C.CH3-![]() -CH3 D.CH3CH2-
-CH3 D.CH3CH2-![]() -OH
-OH
5-2 配位键是一种特殊的共价键,共享电子对完全由一个原子提供。该催化剂分子中的配位键是_____________。
5-3 “金(Ⅲ)配合物”中‘Ⅲ’表示_____________。
5-4 氧化硫醚的氧化剂一般选择过氧化氢,由于副产物是水,对环境十分友好,所以,过氧化氢被称为“绿色氧化剂”。
①过氧化氢与水比较:沸点较高的是________;密度较大的是________;常见分子中,与过氧化氢式量相同的分子是__________(填化学式)。
②过氧化氢可以看作二元弱酸,在低温、稀溶液状态下能较稳定地存在,其水溶液俗称双氧水。请设计一条实验室制备少量纯净的双氧水的合成路线(只写出原理即可)。
③HOF 是较新发现的一种特殊物质,该物质容易水解能得到有氧化性的酸性溶液。请写出该水解方程式________________________。
Ⅰ.大多数的化学反应都是可逆反应。
在一个容积为2.0L的固定容积的密闭容器中,保持一定温度,在一定条件下进行以下反应:A(g)+2B(g) ![]() 3C(g)。向容器中加入2.0molA和6.0 molB,当反应进行到2min时达到平衡,此时生成了3.0molC。
3C(g)。向容器中加入2.0molA和6.0 molB,当反应进行到2min时达到平衡,此时生成了3.0molC。
(1)用B的浓度变化来表示的反应速率u(B)=____。该反应在此条件下的化学平衡常数K=____(结果用分数表示)。
(2)在相同实验条件下,若在同一容器中加入2.0molA和8.0molB,若要求平衡后C在反应混合气中体积分数不变,则还应加入C ____mol。
(3)在相同实验条件下,若在同一容器中加入3.0molA和一定量的B,平衡时C的物质的量为3.0mol,则加入的B的物质的量为____mol
Ⅱ.在含有弱电解质的溶液中,往往有多个化学平衡共存。
(1)常温下,将0.2mol/L的某一元酸HA溶液和0.1mol/L NaOH溶液等体积混合,所得溶液pH大于7,若混合液体积等于两溶液体积之和,则混合液中下列关系正确的是( )
A.c(HA)<c(A―) B.c(HA)一定大于0.1mol/L
C.c(Na+)=c(HA)+c(A―) D.c(OH―)=c(H+)+![]() [c(HA)一c(A―)]
[c(HA)一c(A―)]
(2)常温下,在20mL0.1mol/L![]() 溶液中逐滴加入0.1mol/L HCI溶液40mL,溶液中含碳元素的各种微粒(
溶液中逐滴加入0.1mol/L HCI溶液40mL,溶液中含碳元素的各种微粒(![]() 因逸出未画出)物质的量分数(纵轴)随溶液pH变化的部分情况如下图所示。
因逸出未画出)物质的量分数(纵轴)随溶液pH变化的部分情况如下图所示。

回答下列问题:
①在同一溶液中,![]() ,、
,、![]() 、
、![]() (填:“能”或“不能”)____大量共存。
(填:“能”或“不能”)____大量共存。
②当pH=7时,溶液中各种离子其物质的量浓度之间的等量关系是:____
③已知在![]() 时,
时,![]() 水解反应的平衡常数即水解常数
水解反应的平衡常数即水解常数
![]() ,当溶液中c(
,当溶液中c(![]() ):c(
):c(![]() )=2:1时,溶液的pH:___。
)=2:1时,溶液的pH:___。
(1)合成氨工业对化学工业和国防工业具有重要意义。工业合成氨生产示意图如图甲所示。


①X的化学式为__________,属于________(填“极性”或“非极性”)分子。
 ②图甲中条件选定的主要原因是(选填字母序号,下同)________。
②图甲中条件选定的主要原因是(选填字母序号,下同)________。
A.温度、压强对化学平衡的影响
B.铁触媒在该温度时活性大
C.工业生产受动力、材料、设备等条件的限制
③改变反应条件,会使平衡发生移动。图乙表示随条件改变,氨气的百分含量的变化趋势。当横坐标为压强时,变化趋势正确的是________,当横坐标为温度时,变化趋势正确的是__________。
(2)常温下氨气极易溶于水,其水溶液可以导电。
①用方程式表示氨气溶于水的过程中存在的可逆反应:
___________________________________________________________________。
②氨水中水电离出的c(H+)___________10-7 mol/L(填“>”、“<”或“=”)。
③将氨水和盐酸混合后,某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:
A.c(Cl-)>c(NH4+)>c(H+)>c(OH-) B.c(Cl-)>c(NH4+)>c(OH-)>c(H+)
C.c(Cl-)>c(H+)>c(NH4+)>c(OH-) D.c(NH4+)>c(Cl-)>c(OH-)>c(H+)
Ⅰ、若溶液中只溶解了一种溶质,该溶质的名称是 ,上述离子浓度大小顺序关系中正确的是(选填序号) 。
Ⅱ、若上述关系中C是正确的,则溶液中溶质的化学式是 。
Ⅲ、若该溶液中由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前
c(HCl) c(NH3·H2O)(填“>”、“<”、或“=”,下同),混合后溶液中c(NH4+)与c(Cl-)的关系c(NH4+) c(Cl-)。
(3)氨气具有还原性,在铜的催化作用下,氨气和氟气反应生成X和Y两种物质。X为铵盐,Y在标准状况下为气态。在此反应中,若每反应1体积氨气,同时反应0.75体积氟气;若每反应8.96 L氨气(标准状况),同时生成0.3 mol X。
①写出氨气和氟气反应的化学方程式: ___________________________________。
②在标准状况下,每生成1 mol Y,转移电子的物质的量为___________mol。
(4)已知液态NH3与H2O相似,也可以发生微弱的电离,电离出含有相同电子数的微粒,则液态NH3的电离方程式为:
(1)合成氨工业对化学工业和国防工业具有重要意义。工业合成氨生产示意图如图甲所示。
①X的化学式为__________,属于________(填“极性”或“非极性”)分子。
②图甲中条件选定的主要原因是(选填字母序号,下同)________。
A.温度、压强对化学平衡的影响
B.铁触媒在该温度时活性大
C.工业生产受动力、材料、设备等条件的限制
③改变反应条件,会使平衡发生移动。图乙表示随条件改变,氨气的百分含量的变化趋势。当横坐标为压强时,变化趋势正确的是________,当横坐标为温度时,变化趋势正确的是__________。
(2)常温下氨气极易溶于水,其水溶液可以导电。
①用方程式表示氨气溶于水的过程中存在的可逆反应:
___________________________________________________________________。
②氨水中水电离出的c(H+)___________10-7 mol/L(填“>”、“<”或“=”)。
③将氨水和盐酸混合后,某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:
A.c(Cl-)>c(NH4+)>c(H+)>c(OH-) B.c(Cl-)>c(NH4+)>c(OH-)>c(H+)
C.c(Cl-)>c(H+)>c(NH4+)>c(OH-) D.c(NH4+)>c(Cl-)>c(OH-)>c(H+)
Ⅰ、若溶液中只溶解了一种溶质,该溶质的名称是 ,上述离子浓度大小顺序关系中正确的是(选填序号) 。
Ⅱ、若上述关系中C是正确的,则溶液中溶质的化学式是 。
Ⅲ、若该溶液中由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前
c(HCl) c(NH3·H2O)(填“>”、“<”、或“=”,下同),混合后溶液中c(NH4+)与c(Cl-)的关系c(NH4+) c(Cl-)。
(3)氨气具有还原性,在铜的催化作用下,氨气和氟气反应生成X和Y两种物质。X为铵盐,Y在标准状况下为气态。在此反应中,若每反应1体积氨气,同时反应0.75体积氟气;若每反应8.96 L氨气(标准状况),同时生成0.3 mol X。
①写出氨气和氟气反应的化学方程式: ___________________________________。
②在标准状况下,每生成1 mol Y,转移电子的物质的量为___________mol。
(4)已知液态NH3与H2O相似,也可以发生微弱的电离,电离出含有相同电子数的微粒,则液态NH3的电离方程式为:
(1)合成氨工业对化学工业和国防工业具有重要意义。工业合成氨生产示意图如图甲所示。
①X的化学式为__________,属于________(填“极性”或“非极性”)分子。 ②图甲中条件选定的主要原因是(选填字母序号,下同)________。
②图甲中条件选定的主要原因是(选填字母序号,下同)________。
A.温度、压强对化学平衡的影响
B.铁触媒在该温度时活性大
C.工业生产受动力、材料、设备等条件的限制
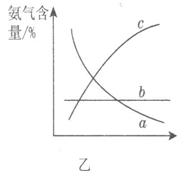
③改变反应条件,会使平衡发生移动。图乙表示随条件改变,氨气的百分含量的变化趋势。当横坐标为压强时,变化趋势正确的是________,当横坐标为温度时,变化趋势正确的是__________。
(2)常温下氨气极易溶于水,其水溶液可以导电。
①用方程式表示氨气溶于水的过程中存在的可逆反应:
___________________________________________________________________。
②氨水中水电离出的c(H+)___________10-7 mol/L(填“>”、“<”或“=”)。
③将氨水和盐酸混合后, 某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:
某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:
A.c(Cl-)>c(NH4+)>c(H+)>c(OH-) B.c(Cl-)>c(NH4+)>c(OH-)>c(H+)
C.c(Cl-)>c(H+)>c(NH4+)>c(OH-) D.c(NH4+)>c(Cl-)>c(OH-)>c(H+)
Ⅰ、若溶液中只溶解了一种溶质,该溶质的名称是 ,上述离子浓度大小顺序关系中正确的是(选填序号) 。
Ⅱ、若上述关系中C是正确的,则溶液中溶质的化学式是 。
Ⅲ、若该溶液中由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前
c(HCl) c(NH3·H2O)(填“>”、“<”、或“=”,下同),混合后溶液中c(NH4+)与c(Cl-)的关系c(NH4+) c(Cl-)。
(3)氨气具有还原性,在铜的催化作用下,氨气和氟气反应生成X和Y两种物质。X为铵盐,Y在标准状况下为气态。在此反应中,若每反应1体积氨气,同时反应0.75体积氟气;若每反应8.96 L氨气(标准状况),同时生成0.3 mol X。
①写出氨气和氟气反应的化学方程式: ___________________________________。
②在标准状况下,每生成1 mol Y,转移电子的物质的量为___________mol。
(4)已知液态NH3与H2O相似,也可以发生微弱的电离,电离出含有相同电子数的微粒,则液态NH3的电离方程式为:
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com