
题目列表(包括答案和解析)
河水里的微生物在使有机物(以C6H10O5表示)转化为CO2和H2O的过程中,所需的O2量叫生化需氧量(BOD),BOD是衡量水体质量的一个指标.
(1)C6H10O5和O2反应生成CO2和H2O是一个氧化还原反应,试写出该反应的化学方程式:________________________.
(2)20℃时,1.0L某水体(假设该水的密度为1g·cm-3)中含有机物(C6H10O5)的质量分数为0.0010%,则该水体的BOD为________________.
(3)20℃时,1.0L水中溶有O2 0.0092g.上述水体是否适合鱼类生存?________,原因是________________.
| 催化剂 |
| 催化剂 |
| ||
| 叶绿体 |
| ||
| 叶绿体 |

| 催化剂 |
| △ |
| 催化剂 |
| △ |
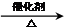 2CH3CHO+2H2O
2CH3CHO+2H2O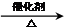 2CH3CHO+2H2O
2CH3CHO+2H2O
| ||
| ||
| ||
| ||
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com