
ƒø¡–±Ì(∞¸¿®¥∞∏∫ÕΩ‚Œˆ)
≈®¡ÚÀ·æþ”–“‘œ¬A°´Fµƒ–‘÷ £∫AÀ·–‘£ªB∏þ∑–µ„ƒ—ª”∑¢£ªCŒ¸ÀÆ–‘£ªDÕ—ÀÆ–‘£ªE«ø—ıªØ–‘£ªF»Ð”⁄ÀÆ∑≈≥ˆ¥Û¡ø»»
(1)≈®¡ÚÀ·”ÎÕ≠π≤»»∑¢…˙∑¥”¶µƒªØ—ß∑Ω≥Ã ΩŒ™ °£ µ—È÷–Õ˘Õ˘”–¥Û¡ø¿∂…´πÃÃÂŒˆ≥ˆ£¨ø…º˚≈®¡ÚÀ·‘⁄∏√ µ—È÷–±Ìœ÷µƒ–‘÷ ”– °£(≈®¡ÚÀ·–‘÷ ”√°∞A°±°¢°∞B°±°¢°∞C°±°¢°∞D°±°¢°∞E°±°¢°∞F°±ÃÓø’£¨œ¬Õ¨)
(2) µ—È÷§√˜Õ≠≤ªƒÐ‘⁄µÕŒ¬œ¬”ÎO2∑¥”¶£¨“≤≤ªƒÐ”Îœ°¡ÚÀ·π≤»»∑¢…˙∑¥”¶£¨µ´π§“µ…œ»¥ «Ω´∑œÕ≠–ºµπ»Î»»µƒœ°¡ÚÀ·÷–≤¢Õ®»Îø’∆¯¿¥÷∆±∏CuSO4»Ð“∫°£Õ≠–º‘⁄¥À◊¥Ã¨œ¬±ª»ÐΩ‚µƒªØ—ß∑Ω≥Ã ΩŒ™ °£¡ÚÀ·‘⁄∏√∑¥”¶÷–±Ìœ÷µƒ–‘÷ « °£
(3)‘⁄π˝—ıªØ«‚”Îœ°¡ÚÀ·µƒªÏ∫œ»Ð“∫÷–º”»ÎÕ≠∆¨£¨≥£Œ¬œ¬æÕ…˙≥…¿∂…´»Ð“∫°£–¥≥ˆ”–πÿ∑¥”¶µƒªØ—ß∑Ω≥Ã Ω£∫ °£”Î(2)÷–∑¥”¶±»Ωœ£¨∑¥”¶Ãıº˛≤ªÕ¨µƒ‘≠“Ú « °£
(4)œÚ’·Ã«æßÃÂ÷–µŒ2°´3µŒÀÆ£¨‘ŸµŒ»Î ¡øµƒ≈®¡ÚÀ·°£∑¢œ÷º”ÀÆ¥¶¡¢º¥±‰∫⁄£¨∫⁄…´«¯≤ª∂œ¿©¥Û£¨◊Ó∫Û±‰≥…“ªøÈ ËÀ…µƒΩπÃø£¨≤¢∞È”–¥Ãº§–‘∆¯Œ∂µƒ∆¯ÃÂ≤˙…˙°£–¥≥ˆ≤˙…˙”–¥Ãº§∆¯Œ∂∆¯ÃµƒªØ—ß∑Ω≥Ã Ω£∫ °£∏√ µ—È÷–≈®¡ÚÀ·±Ìœ÷µƒ–‘÷ ”– °£
¡ÚÀ·æþ”–“‘œ¬A°´Fµƒ–‘÷ £∫A.À·–‘°°B£Æ∏þ∑–µ„ƒ—ª”∑¢°°C£ÆŒ¸ÀÆ–‘°°D£ÆÕ—ÀÆ–‘°°E£Æ«ø—ıªØ–‘°°F£Æ»Ð”⁄ÀÆ∑≈≥ˆ¥Û¡ø»»
(1)≈®¡ÚÀ·”ÎÕ≠π≤»»∑¢…˙∑¥”¶µƒªØ—ß∑Ω≥Ã ΩŒ™____________°£ µ—È÷–Õ˘Õ˘”–¥Û¡ø∞◊…´πÃÃÂŒˆ≥ˆ£¨ø…º˚≈®¡ÚÀ·‘⁄∏√ µ—È÷–±Ìœ÷¡Àƒƒ–©–‘÷ £∫____________°£(≈®¡ÚÀ·–‘÷ ”√A°¢B°¢C°¢D°¢E°¢FÃÓø’£¨œ¬Õ¨)
(2) µ—È÷§√˜Õ≠≤ªƒÐ‘⁄µÕŒ¬œ¬”ÎO2∑¥”¶£¨“≤≤ªƒÐ”Îœ°H2SO4π≤»»∑¢…˙∑¥”¶£¨µ´π§“µ…œ»¥ «Ω´∑œÕ≠–ºµπ»Î»»µƒœ°H2SO4÷–≤¢Õ®»Îø’∆¯¿¥÷∆±∏CuSO4»Ð“∫°£Õ≠–º‘⁄¥À◊¥Ã¨œ¬±ª»ÐΩ‚µƒªØ—ß∑Ω≥Ã ΩŒ™__________________________________°£¡ÚÀ·‘⁄∏√∑¥”¶÷–±Ìœ÷¡Àƒƒ–©–‘÷ £∫____________________________°£
(3)‘⁄π˝—ıªØ«‚∏˙œ°¡ÚÀ·µƒªÏ∫œ»Ð“∫÷–º”»ÎÕ≠∆¨£¨≥£Œ¬œ¬æÕ…˙≥…¿∂…´»Ð“∫°£–¥≥ˆ”–πÿ∑¥”¶µƒªØ—ß∑Ω≥Ã Ω£∫____________°£”Î(2)÷–∑¥”¶±»Ωœ∑¥”¶Ãıº˛≤ªÕ¨µƒ‘≠“Ú «____________°£
(4)’·Ã«æßÃÂ÷–µŒ2°´3µŒÀÆ£¨‘ŸµŒ»Î ¡øµƒ≈®¡ÚÀ·°£∑¢œ÷º”ÀÆ¥¶¡¢º¥±‰∫⁄£¨∫⁄…´«¯≤ª∂œ¿©¥Û£¨◊Ó∫Û±‰≥…“ªøÈ ËÀ…µƒΩπÃø£¨≤¢∞È”–¥Ãº§–‘∆¯Œ∂∆¯ÃÂ≤˙…˙°£–¥≥ˆ≤˙…˙”–¥Ãº§∆¯Œ∂∆¯ÃµƒªØ—ß∑Ω≥Ã Ω£∫____________________________°£∏√ µ—È÷–≈®¡ÚÀ·±Ìœ÷µƒ–‘÷ ”–____________________°£
(5)𧓵÷∆±∏CuSO4»Ð“∫≤…”√ µ—È(2)µƒ‘≠¿Ì∂¯√ª”–≤…”√ µ—È(1)∫Õ(3)µƒ‘≠¿Ì£¨ «“ÚŒ™(1)∫Õ(3)”–ƒ≥–©»±µ„£¨«Îƒ„¡–æŸ(1)∫Õ(3)∑÷±”–ƒƒ¥À»±µ„£∫ µ—È(1)____________________________£ª µ—È(3)____________________________°£
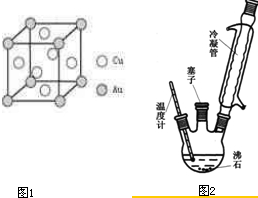
‘À”√ªØ—ß∑¥”¶‘≠¿Ì—–æøú°¢µ™°¢¡Ú°¢¬»µ»µ•÷ º∞∆‰ªØ∫œŒÔµƒ∑¥”¶£¨∂‘…˙≤˙°¢…˙ªÓ°¢ª∑æ≥±£ª§µ»¡Ï”Ú”–◊≈÷ÿ“™µƒ“‚“°£
£®1£©œ¬¡–¥Î ©÷–£¨≤ª¿˚”⁄ª∑æ≥±£ª§µƒ”– £®ÃÓ±ý∫≈£©°£
a.¥Û¡øø™≤… π”√ªØ Ø»º¡œ
b. π”√ŒÞ∑˙±˘œ‰°¢ø’µ˜
c.∂ý≤Ω––∂ý≥Àπ´Ωª≥µ£¨…Ÿ”√◊®≥µ∫ÕÀΩº“≥µ
d.Ω´π§“µ°∞∑œ∆¯°±°¢°∞∑œ“∫°±°¢°∞∑œ‘¸°±÷±Ω”≈≈∑≈
£®2£©π§“µ…œµƒ°∞՗ú°±÷∏µƒ «¥”°∞Õ—œı°±°¢°∞Õ—¡Ú°±∫Ûµƒ—Ã∆¯”√ºÓ“∫Œ¸ ’≤¢µ√µΩ≈®Àıµƒ∂˛—ıªØú°£¿˚”√∂˛—ıªØú∫œ≥…º◊¥º «Ãººı≈≈µƒ–¬∑ΩœÚ°£
¢Ÿ–¥≥ˆŒ¸ ’∂˛—ıªØúµƒ¿Î◊”∑Ω≥Ã Ω °£
¢⁄≥£Œ¬œ¬£¨0.1mol/LNaHCO3»Ð“∫µƒpH£æ8£¨‘ڻГ∫÷–c(H2CO3) _______c(CO32£≠) £®ÃÓ°∞£æ°±°¢°∞£º°±ªÚ°∞£Ω°±£©°£
¢€∫œ≥…µƒº◊¥ºø…“‘◊ˆŒ™–¬–Õ»º¡œµÁ≥ÿµƒ‘≠¡œ£¨»ÙµÁΩ‚“∫ «ºÓ–‘µƒ£¨‘Ú∆‰∏∫º´µƒµÁº´∑¥”¶ ΩŒ™ °£
£®3£©∂˛—ıªØ¬»£®ClO2£©£¨Œ™“ª÷÷ª∆¬Ã…´∆¯Ã£¨ «π´»œµƒ∏þ–ß°¢π„∆◊∞≤»´µƒ…±æ˙œ˚∂溡°£π§“µ…œ÷∆±∏ClO2µƒ∑¥”¶‘≠¿ÌŒ™£∫4HC1(≈®)+2NaClO3£Ω2ClO2°¸+Cl2°¸+2H2O+2NaCl°£…œ ˆ∑¥”¶÷–£¨≤˙…˙1 mol ClO2£¨‘Ú±ª—ıªØµƒHC1Œ™ °£
£®4£©SO2»Ð”⁄ÀÆø…“‘µ√µΩ∂˛‘™»ıÀ·H2SO3£®—«¡ÚÀ·£©°£
¢Ÿ25°Ê ±£¨Ω´NaOH…Ó“∫”Η«¡ÚÀ·ªÏ∫œ÷¡«°∫√÷–∫Õ£¨‘ÚªÏ∫œ“∫÷–∏˜÷÷¿Î◊”≈®∂»µƒ¥Û–°πÿœµŒ™ °£
¢⁄25°Ê ±£¨µ±NaOH»Ð“∫”ÎH2SO3µ»ŒÔ÷ µƒ¡øªÏ∫œ ±£¨∑¢œ÷ªÏ∫œ“∫pH£º7£¨«Îƒ„ºÚ“™Ω‚ Õ∆‰‘≠“Ú °£
‘À”√ªØ—ß∑¥”¶‘≠¿Ì—–æøú°¢µ™°¢¡Ú°¢¬»µ»µ•÷ º∞∆‰ªØ∫œŒÔµƒ∑¥”¶£¨∂‘…˙≤˙°¢…˙ªÓ°¢ª∑æ≥±£ª§µ»¡Ï”Ú”–◊≈÷ÿ“™µƒ“‚“°£
£®1£©œ¬¡–¥Î ©÷–£¨≤ª¿˚”⁄ª∑æ≥±£ª§µƒ”– £®ÃÓ±ý∫≈£©°£
a.¥Û¡øø™≤… π”√ªØ Ø»º¡œ
b. π”√ŒÞ∑˙±˘œ‰°¢ø’µ˜
c.∂ý≤Ω––∂ý≥Àπ´Ωª≥µ£¨…Ÿ”√◊®≥µ∫ÕÀΩº“≥µ
d.Ω´π§“µ°∞∑œ∆¯°±°¢°∞∑œ“∫°±°¢°∞∑œ‘¸°±÷±Ω”≈≈∑≈
£®2£©π§“µ…œµƒ°∞՗ú°±÷∏µƒ «¥”°∞Õ—œı°±°¢°∞Õ—¡Ú°±∫Ûµƒ—Ã∆¯”√ºÓ“∫Œ¸ ’≤¢µ√µΩ≈®Àıµƒ∂˛—ıªØú°£¿˚”√∂˛—ıªØú∫œ≥…º◊¥º «Ãººı≈≈µƒ–¬∑ΩœÚ°£
¢Ÿ–¥≥ˆŒ¸ ’∂˛—ıªØúµƒ¿Î◊”∑Ω≥Ã Ω °£
¢⁄≥£Œ¬œ¬£¨0.1mol/LNaHCO3»Ð“∫µƒpH£æ8£¨‘ڻГ∫÷–c(H2CO3) _______c(CO32£≠) £®ÃÓ°∞£æ°±°¢°∞£º°±ªÚ°∞£Ω°±£©°£
¢€∫œ≥…µƒº◊¥ºø…“‘◊ˆŒ™–¬–Õ»º¡œµÁ≥ÿµƒ‘≠¡œ£¨»ÙµÁΩ‚“∫ «ºÓ–‘µƒ£¨‘Ú∆‰∏∫º´µƒµÁº´∑¥”¶ ΩŒ™ °£
£®3£©∂˛—ıªØ¬»£®ClO2£©£¨Œ™“ª÷÷ª∆¬Ã…´∆¯Ã£¨ «π´»œµƒ∏þ–ß°¢π„∆◊∞≤»´µƒ…±æ˙œ˚∂溡°£π§“µ…œ÷∆±∏ClO2µƒ∑¥”¶‘≠¿ÌŒ™£∫4HC1(≈®)+2NaClO3£Ω2ClO2°¸+Cl2°¸+2H2O+2NaCl°£…œ ˆ∑¥”¶÷–£¨≤˙…˙1 mol ClO2£¨‘Ú±ª—ıªØµƒHC1Œ™ °£
£®4£©SO2»Ð”⁄ÀÆø…“‘µ√µΩ∂˛‘™»ıÀ·H2SO3£®—«¡ÚÀ·£©°£
¢Ÿ25°Ê ±£¨Ω´NaOH…Ó“∫”Η«¡ÚÀ·ªÏ∫œ÷¡«°∫√÷–∫Õ£¨‘ÚªÏ∫œ“∫÷–∏˜÷÷¿Î◊”≈®∂»µƒ¥Û–°πÿœµŒ™ °£
¢⁄25°Ê ±£¨µ±NaOH»Ð“∫”ÎH2SO3µ»ŒÔ÷ µƒ¡øªÏ∫œ ±£¨∑¢œ÷ªÏ∫œ“∫pH£º7£¨«Îƒ„ºÚ“™Ω‚ Õ∆‰‘≠“Ú °£
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com