
题目列表(包括答案和解析)
氯碱厂电解饱和食盐水制取NaOH的工艺流程示意图如下:
依据工艺流程图,完成下列填空。
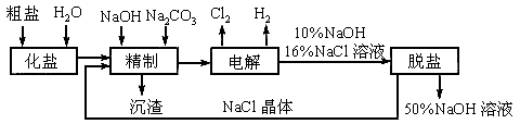
(1)在电解过程中,与电源正极相连的电极上发生反应的电极方程式为_______________,
与电源负极相连的电极附近,溶液pH________;(填“不变”、“升高”或“下降”)
(2)工业食盐含Ca2+、Mg2+等杂质。精制过程发生反应的离子方程式为________________,________________;
(3)如果粗盐中![]() 含量较高,必须添加钡试剂除去
含量较高,必须添加钡试剂除去![]() ,该钡试剂可以是________;(填序号)
,该钡试剂可以是________;(填序号)
a.Ba(OH)2 b.Ba(NO)2 c.BaCl2
(4)为了有效去除Ca2+、Mg2+、![]() ,加入试剂的合理顺序为________;(填序号)
,加入试剂的合理顺序为________;(填序号)
a.先加NaOH,后加Na2CO3,再加钡试剂
b.先加NaOH,后加钡试剂,再加Na2CO3
c.先加钡试剂,后加NaOH,再加Na2CO3
(5)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过________、冷却、________(填写操作名称)除去NaCl;
(6)用隔膜法电解食盐水时,电解槽分隔为阳极区和阴极区,防止Cl2与NaOH反应。采用无隔膜电解冷的食盐水时,Cl2与NaOH充分接触,产物仅是NaClO和H2,相应的化学方程式为________________________________。
依据工艺流程图,完成下列填空。
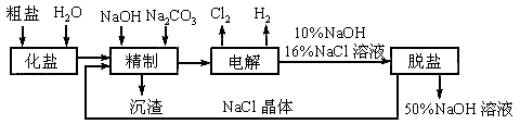
(1)在电解过程中,与电源正极相连的电极上发生反应的电极方程式为_______________,
与电源负极相连的电极附近,溶液pH________;(填“不变”、“升高”或“下降”)
(2)工业食盐含Ca2+、Mg2+等杂质。精制过程发生反应的离子方程式为________________,________________;
(3)如果粗盐中![]() 含量较高,必须添加钡试剂除去
含量较高,必须添加钡试剂除去![]() ,该钡试剂可以是________;(填序号)
,该钡试剂可以是________;(填序号)
a.Ba(OH)2 b.Ba(NO)2 c.BaCl2
(4)为了有效去除Ca2+、Mg2+、![]() ,加入试剂的合理顺序为________;(填序号)
,加入试剂的合理顺序为________;(填序号)
a.先加NaOH,后加Na2CO3,再加钡试剂
b.先加NaOH,后加钡试剂,再加Na2CO3
c.先加钡试剂,后加NaOH,再加Na2CO3
(5)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过________、冷却、________(填写操作名称)除去NaCl;
(6)用隔膜法电解食盐水时,电解槽分隔为阳极区和阴极区,防止Cl2与NaOH反应。采用无隔膜电解冷的食盐水时,Cl2与NaOH充分接触,产物仅是NaClO和H2,相应的化学方程式为________________________________。
依据工艺流程图,完成下列填空。
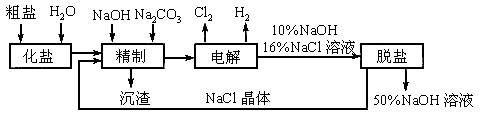
(1)在电解过程中,与电源正极相连的电极上发生反应的电极方程式为_______________,
与电源负极相连的电极附近,溶液pH________;(填“不变”、“升高”或“下降”)
(2)工业食盐含Ca2+、Mg2+等杂质。精制过程发生反应的离子方程式为________________,
________________;
(3)如果粗盐中![]() 含量较高,必须添加钡试剂除去
含量较高,必须添加钡试剂除去![]() ,该钡试剂可以是________;(填序号)
,该钡试剂可以是________;(填序号)
a.Ba(OH)2 b.Ba(NO)2 c.BaCl2
(4)为了有效去除Ca2+、Mg2+、![]() ,加入试剂的合理顺序为________;(填序号)
,加入试剂的合理顺序为________;(填序号)
a.先加NaOH,后加Na2CO3,再加钡试剂
b.先加NaOH,后加钡试剂,再加Na2CO3
c.先加钡试剂,后加NaOH,再加Na2CO3
(5)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过________、冷却、________(填写操作名称)除去NaCl;
(6)用隔膜法电解食盐水时,电解槽分隔为阳极区和阴极区,防止Cl2与NaOH反应。采用无隔膜电解冷的食盐水时,Cl2与NaOH充分接触,产物仅是NaClO和H2,相应的化学方程式为________________________________。
氯碱厂电解饱和食盐水制取NaOH的工艺流程示意图如下:
依据工艺流程图,完成下列填空。
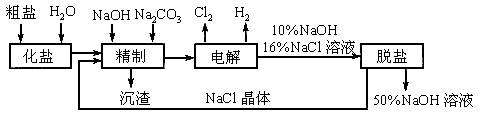
(1)在电解过程中,与电源正极相连的电极上发生反应的电极方程式为_______________,
与电源负极相连的电极附近,溶液pH________;(填“不变”、“升高”或“下降”)
(2)工业食盐含Ca2+、Mg2+等杂质。精制过程发生反应的离子方程式为________________,
________________;
(3)如果粗盐中![]() 含量较高,必须添加钡试剂除去
含量较高,必须添加钡试剂除去![]() ,该钡试剂可以是________;(填序号)
,该钡试剂可以是________;(填序号)
a.Ba(OH)2 b.Ba(NO)2 c.BaCl2
(4)为了有效去除Ca2+、Mg2+、![]() ,加入试剂的合理顺序为________;(填序号)
,加入试剂的合理顺序为________;(填序号)
a.先加NaOH,后加Na2CO3,再加钡试剂
b.先加NaOH,后加钡试剂,再加Na2CO3
c.先加钡试剂,后加NaOH,再加Na2CO3
(5)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过________、冷却、________(填写操作名称)除去NaCl;
(6)用隔膜法电解食盐水时,电解槽分隔为阳极区和阴极区,防止Cl2与NaOH反应。采用无隔膜电解冷的食盐水时,Cl2与NaOH充分接触,产物仅是NaClO和H2,相应的化学方程式为________________________________。
设阿伏加德罗常数的数值为NA,下列说法正确的是
A.28g乙烯分子中含有极性共价键的数目为6NA
B.一定条件下,0.1molCu与0.1molI2充分反应,转移的电子数一定为0.2NA
C.标准状况下,11.2L以任意比例混合的NO和O2的混合气体中所含原子个数为NA
D.25℃时,pH=13的1.0 L Ba(OH)2溶液中含有的OH-数目为0.2NA
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com