
题目列表(包括答案和解析)
在H2、O2、NH3、Cl2、HCl、H2S、SO2、CO2、NO、NO2、CH4、C2H4、C2H2等气体中:
(1)在实验室中,可用启普发生器制取的气体是________.
(2)可用排水集气法收集的气体有________.
(3)不宜用排空气集气法收集的气体有________.
(4)可以用瓶口向上排空气集气法收集的气体有________.
(5)实验室制取上述气体时,制气装置
①可与制O2装置相同的有________.
②可与制Cl2装置相同的有________.
③可与制CO2装置相同的有________.
(6)通常用H2SO4和另一种物质反应制取的有________.
(7)极易溶于水,可做“喷泉实验”的气体有________.
(8)有刺激性气味的气体有________.
(9)有颜色的气体有________.
(10)在空气中可以燃烧的有________.
A.HBr、CO2、Cl2、 CO B.H2S、SO3、 Cl2、NO
C.H2S、SO2、Cl2 、NO D.HCl、NO2 、Cl2 、NO
甲、乙、丙、丁在常温下为四种气体,它们都是大气污染物。其中甲的水溶液是一种无氧酸,乙是形成酸雨的主要物质,丙可以跟甲发生氧化还原反应,丁能与血红蛋白作用而使人体中毒。则甲、乙、丙、丁依次为( )
A.HBr、CO2、Cl2、 CO B.H2S、SO3、 Cl2、NO
C.H2S、SO2、Cl2 、NO D.HCl、NO2 、Cl2 、NO
 ______2(填“>”“<”或“=”)
______2(填“>”“<”或“=”)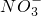 还原为NO,写出该过程中产生NO反应的离子方程式______.
还原为NO,写出该过程中产生NO反应的离子方程式______.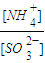 ______2(填“>”“<”或“=”)
______2(填“>”“<”或“=”) 还原为NO,写出该过程中产生NO反应的离子方程式______.
还原为NO,写出该过程中产生NO反应的离子方程式______.湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com