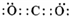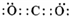A、B、C、D、E、F、G七种短周期元素的原子序数依次增大.A和E最外层电子数相同,短周期主族元素的原子中,E原子的半径最大;B、C和F在周期表中相邻,B、C同周期,C、F同主族,F原子的质子数是C原子质子数的2倍;A和C可形成两种常见的液态化合物X和Y(相对分子质量X<Y );D形成的分子为单原子分子.回答问题:
(1)D元素的名称为
氖
氖
,F形成的离子的结构示意图为
.
(2)写出液态化合物Y的一种用途
一定浓度的H2O2溶液作消毒剂
一定浓度的H2O2溶液作消毒剂
.
(3)用某种金属易拉罐与A、C、E组成的化合物的水溶液反应,产生的气体可充填气球,请写出该反应的离子方程式
2Al+2OH-+2H2O=2AlO2-+3H2↑
2Al+2OH-+2H2O=2AlO2-+3H2↑
,使用这种气球存在的隐患是
易燃、易爆
易燃、易爆
.
(4)P和Q两种物质都是由A、C、E、F四种元素组成的盐,其水溶液都显酸性,等物质的量的P和Q恰好完全反应.写出该反应的离子方程式:
H++HSO3-=H2O+SO2↑
H++HSO3-=H2O+SO2↑
.
(5)由A、B两元素形成的化合物W可作为火箭推进器中的强还原剂,已知一个W分子和一个Y分子中都含有18个电子,0.5mol液态W和足量液态Y反应,生成一种无色无味无毒的气体B
2和液态X,并放出408.8kJ热量.查资料可知:
2Y(1)=2X(1)+C
2(g)△H=-196.4kJ?mol
-1写出液态W与气态C
2反应生成液态X和气态B
2的热化学方程式为
N2H4(1)+O2(g)=N2(g)+2H2O(1)△H=-621.2kJ?mol-1
N2H4(1)+O2(g)=N2(g)+2H2O(1)△H=-621.2kJ?mol-1
.该反应还可设计为原电池(以KOH溶液为电解质溶液),请写出该电池的负极反应式:
N2H4-4e-+4OH-=N2+4H2O
N2H4-4e-+4OH-=N2+4H2O
.
(6)G为氯,以K
2CrO
4为指示剂,用标准硝酸银溶液可以测定溶液中Cl
-的浓度,已知Ksp(AgCl)=1.56ⅹ10
-10,Ksp(Ag
2CrO
4)=1.10ⅹ10
-12,Ag
2CrO
4为砖红色,则滴定终点的现象是
滴入最后一滴硝酸银溶液时,溶液中出现砖红色深沉,振荡后砖红色沉淀不溶解
滴入最后一滴硝酸银溶液时,溶液中出现砖红色深沉,振荡后砖红色沉淀不溶解
.




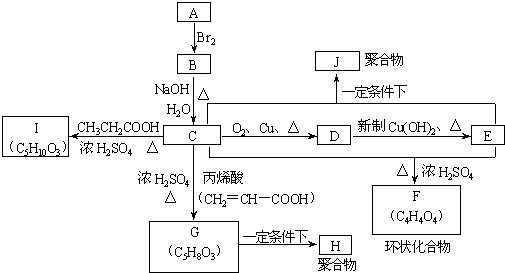


 +(2n-1)H2O
+(2n-1)H2O +(2n-1)H2O
+(2n-1)H2O

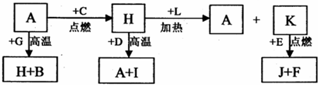 A、B、C、D、E、F 是常见单质,其中 A 是用量最大,应用最广泛的金属;元素 D 是地壳中含量最多的金属元素:D 元素和 E 元素在周期表中相邻,G、H、l、J、K、L 是常见化合物,其中 G 在常温下是无色液体,H 是黑色晶体,以上物质相互间的转化关系如图所示:
A、B、C、D、E、F 是常见单质,其中 A 是用量最大,应用最广泛的金属;元素 D 是地壳中含量最多的金属元素:D 元素和 E 元素在周期表中相邻,G、H、l、J、K、L 是常见化合物,其中 G 在常温下是无色液体,H 是黑色晶体,以上物质相互间的转化关系如图所示: