
题目列表(包括答案和解析)
已知在一个NaCl晶胞中含有4个Na+和4个Cl-,且一个NaCl晶胞体积为8a3cm3在实验室中可用NaCl来精确测定阿伏加德罗常数(NA),其步骤如下:
①将固体NaCl细粒干燥后,准确称取m g NaCl固体并转移到定容仪器A中;
②用滴定管向A仪器中加苯,不断振荡,继续加苯到A仪器的刻度,计算出NaCl固体的体积V cm3。求算阿伏加德罗常数
请回答下列问题:
(1)步骤①中A仪器最好使用____________(填序号)。
A.量筒 B.烧杯 C.容量瓶 D.试管
(2)本实验中滴定管应选____________滴定管(填“酸式”式“碱式”),原因____________
____________ 。
(3)能否用水代替苯____________,理由____________
____________ 。
(4)NA表达式为____________ 。
NaCl的晶胞如图所示,将NaCl晶胞中的所有Cl-去掉,并将Na+全部换成C原子,再在晶胞的4个“小立方体”中心处各放置一个C原子,且这四个“小立方体”互不共面,位于“小立方体”中的碳原子均与最近的4个碳原子成键,以此表示金刚石的一个晶胞。若再将在成键的C原子中心联线的中点处增添一个O原子,则构成了某种CO2的晶胞。则下面说法正确的是( )(已知C-C键的键长1.54×10-10m)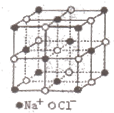
| A.一个金刚石的晶胞中有8个C原子 |
| B.金刚石的密度为3.54g·cm-1 |
| C.在该种CO2晶体中,一个CO2分子由一个C原子和二个氧原子构成 |
| D.在该种CO2晶胞中含氧原子8个 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com